FISTULA ANAL
La
fistula anal es el proceso crónico secundario al drenaje de un absceso anal, en
el cual se establece un trayecto epitelizado entre el conducto anal o el recto
(orificio primario) y la piel perianal (orificio secundario).
Una
mayor incidencia en hombres, con un pico de edad de presentación entre los 30 a
50 años, con una incidencia global de 2 por 10 000.
El
paciente acude al médico por la salida de pus a través del orificio secundario,
de manera intermitente, presentando en ocasiones dolor y fiebre por
exacerbaciones de un absceso cuando el orificio secundario se ocluye. El
paciente se coloca gasas u otros protectores por el drenaje purulento, el cual
es maloliente. Todo esto genera alteraciones importantes en la calidad de vida
del portador del padecimiento.
La
teoría criptoglandular propone como etiología del absceso y la fistula anal la
infección de las glándulas del conducto anal, localizadas a nivel de la linea
anorrectal o dentada dentro del espacio interesfintérico. Este origen se
menciona como inespecífico y es la causante en 95% de los pacientes con fistula
anal. El origen específico de las fístulas es: secundarias a enfermedad
inflamatoria intestinal (enfermedad de Crohn); infecciosas (tuberculosis,
actinomicosis, linfogranuloma venéreo); secundarias a traumatismos
(empalamiento, introducción de cuerpos extraños); posteriores a cirugías
(episiotomia, hemorroidectomia, prostatectomia); a enfermedad neoplásica
(cáncer de recto, cáncer de ano, leucemia y linfomas), y posterior a
radioterapia.
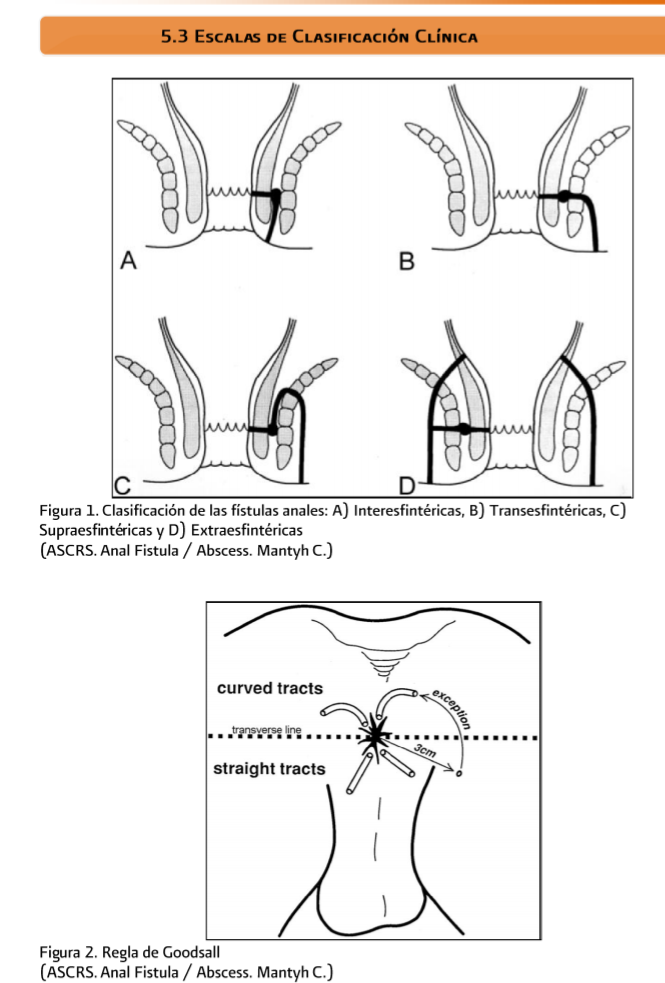
La
clasificación clínica actual de las fistulas anales fue propuesta por Sir Allan
Parks del Hospital St. Marks en 1967, basada en su estudio de 400 pacientes, en
el que concluye que hay cuatro tipos básicos: interesfintéricas, transesfintéricas,
extraesfintéricas y supraesfintéricas.
Éstas
se pueden subclasificar de acuerdo con extensiones o trayectos secundarios. El
45% de las fistulas son interesfintéricas 29%, transesfintéricas 20%,
supraesfintéricas, y 5%, extraesfintéricas. A éstas agregamos algunas
variantes, como los trayectos superficiales o submucosos y las fistulas en
herradura.
Por
otra parte, una fistula puede ser llamada compleja cuando su trayecto
compromete por más de 30% a 50% del esfinter externo (transesfintérica alta,
supraesfintérica o extraesfintérica), es de localización anterior en mujeres,
el paciente se encuentra con algún grado de incontinencia, existe enfermedad
inflamatoria intestinal (eg. Enfermedad de Crohn) o tiene el antecedente de
cirugias previas de la región anorrectal (e.g. fistulas recurrentes). El tener
múltiples trayectos no necesariamente implica complejidad, ya que los mismos
pueden ser superficiales y no comprometer el complejo esfinteriano; sin
embargo, éstas fistulas deben contar con algún estudio de gabinete.
Las
fistulas se tratan quirúrgicamente de acuerdo con la clasificación del trayecto
principal (clasificación de Parks), y según su complejidad. El término de
"complejo" prevalecerá para un correcto tratamiento sobre la
localización del trayecto principal.
La
fistulotomia es el procedimiento más utilizado, ya que la mayor parte de las
fistulas anales son interesfintéricas o transesfintéricas bajas. Debemos
considerar que una fistula interesfintérica en un paciente con algún grado de
incontinencia debe tratarse como si fuera compleja, sin importar la
localización del trayecto principal. Sin embargo, la fistulotomía no está
exenta de ocasionar en algunos pacientes trastornos menores de la continencia
fecal (soiling). El tratamiento de las fistulas complejas requiere un amplio
conocimiento anatómico y fisiológico de la región anorrectal, para evitar
complicaciones como la incontinencia y la recurrencia.
Los
objetivos del tratamiento de la fistula anal son eliminarla, prevenir la recurrencia
y preservar la función del esfinter anal. Los objetivos secundarios son
minimizar los defectos de cicatrización y ofrecer al paciente una recuperación
rápida, los cuales, con algunas técnicas recientes, se pueden ofrecer al
paciente.
Las
técnicas utilizadas para el tratamiento de la fistula anal se clasifican en
preservadoras y no preservadoras de la continencia fecal. Dentro de las
preservadoras de la continencia fecal las más utilizadas son la fistulotomía,
fistulectomía y setón de corte. Estas son empleadas en fistulas simples,
generalmente. Las técnicas preservadoras de la continencia fecal son: la
fistulectomia con reparación de esfinteres, setón de drenaje, avance de colgajo
de mucosa rectal, aplicación de fibrina, tapón de colágeno biodegradable, termo
obliteración, tratamiento de la fistula anal video asistido, entre otras. Es de
especial interés en las fistulas complejas tener en mente el balance entre la
curación y recurrencia contra preservación de una mejor función del complejo
esfinteriano.
En el
contexto anterior, se debe informar al paciente las opciones y su preferencia
en cuanto a una cirugia preservadora de la continencia con menores
posibilidades de curación y una mayor recurrencia en contraparte con una
cirugia no preservadora de la continencia, la cual tiene mayor éxito para
curación y menor posibilidad de recurrencia, pero el trastorno de la
continencia fecal puede ser importante.
Posterior
al tratamiento de la fistula anal, la utilización de terapia con antibióticos
no es necesaria en todos los pacientes, se limita a una población seleccionada,
generalmente aquéllos con inmunocompromiso. Los trastornos posoperatorios de la
continencia fecal pueden ser menores o constituir una incontinencia marcada. Se
debe recordar que no sólo la continencia fecal es dependiente de la estructura
del complejo esfinteriano, también se encuentra involucrada la sensibilidad
rectal y las caracteristicas de las heces. Habitualmente con el tiempo llega a
mejorar este trastorno y sólo eventualmente se emplea la electroestimulación,
bioretroalimentación o una reparación del esfinter anal para corregirlo.
La
fistula anal es una enfermedad caracterizada por la presencia de un conducto de
paredes fibrosas infectadas que comunica una cripta anal o el lumen del recto
con la piel. El orificio localizado en la cripta anal se denomina primario o
interno, y el cutáneo, secundario o externo.
Las
fistulas simples son generalmente interesfintéricas o transesfintéricas bajas,
generalmente con un trayecto único entre el orificio primario y el secundario.
La fistula compleja tiene un trayecto que compromete más de 30% a 50% del
esfinter externo (transesfintérica alta, supraesfintérica o extraesfintérica),
es de localización anterior en mujeres, la padece un paciente con
incontinencia, existe enfermedad inflamatoria intestinal o el antecedente de
cirugias previas anorrectales.
Las fistulas anales son más comunes en hombres que en mujeres y la frecuencia de presentación es mayor entre los 30 y 50 años de edad.
Las fistulas anales no específicas tiene su origen en la infección de las glándulas que se encuentran en el espacio interesfintérico. A la fecha no hay un factor claro por el cual se inicia este proceso.
La extensión de la infección a partir de la glándula anal puede tener tres direcciones:
1) distal para formar un absceso perianal en la etapa aguda y una fistula interesfintérica en la fase crónica.
2) lateral, penetrando el esfinter externo para crear un absceso isquio-rectal en la fase aguda y una fistula transesfintérica en la crónica.
3)
próxima, lo cual es poco frecuente, para establecer un absceso pélvico en el
espacio supraelevador o un absceso intramuscular alto, dependiendo de la
relación que guarde la glándula infectada con el músculo longitudinal.
En una
pequeña proporción de pacientes, la sepsis es resultado de enfermedades
especificas, como la enfermedad de Crohn, la tuberculosis, el VIH, la
hidradenitis supurativa, entre otras. Diversas condiciones que pueden
manifestarse como fistulas son el linfogranuloma venéreo, el teratoma
sacrococcigeo, la duplicación rectal, la actinomicosis perianal, el trauma por
cuerpos extraños y el cáncer rectal y anal perforado
Existe
evidencia no concluyente sobre los factores de riesgo para el desarrollo de la
fistula posterior al drenaje de un absceso, como el tabaquismo, la diabetes
mellitus, la edad y el VIH.
La utilización de antibióticos para prevenir el desarrollo de una fistula anal posterior al drenaje de un absceso no está justificada.
El tratamiento quirúrgico de la fistula anal requiere del conocimiento detallado de la anatomía, tomando como referencias el piso pélvico y el esfínter anal.
La
historia clínica debe identificar síntomas que sugieran una asociación con
patología intestinal y eventos previos que puedan comprometer la función del
esfínter, como cirugía anorrectal o trauma obstétrico.
Se
deben investigar antecedentes de enfermedades intestinales y descartar
enfermedad inflamatoria intestinal, sobre todo enfermedad de Crohn, además de
procesos infecciosos, como tuberculosis y VIH y antecedentes de hidradenitis
supurativa.
El
orificio secundario (externo) frecuentemente se identifica en la piel perianal
o perineal como un área pequeña invaginada de tejido de granulación con salida
de material purulento o sangre a la compresión digital.
El
trayecto fistuloso puede en ocasiones palparse como un cordón del orificio
secundario hacia el conducto anal; cuando se puede palpar generalmente se trata
de un trayecto superficial. La exploración digital puede identificar el
orificio primario (interno) y la presencia de trayectos fistulosos secundarios.
La identificación correcta del orificio fistuloso primario es la clave para el
tratamiento correcto de la enfermedad. El orificio primario se palpa como una
induración en el tercio medio del conducto anal.
La
anoscopia y la proctoscopia son complementos importantes en la exploración
física de los pacientes con fistula anal, dado que documentan la localización
del orificio primario y la presencia de otras condiciones patológicas, como la
enfermedad inflamatoria intestinal
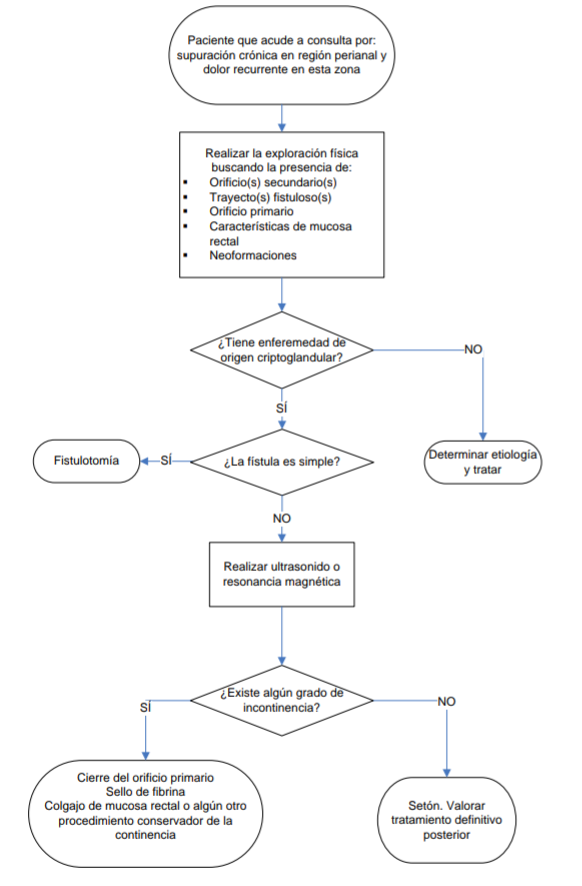
La
regla de Goodsall es correcta en 90% de los casos cuando se aplica a los
orificios secundarios posteriores a la linea anal transversal; sin embargo,
solamente es cierta en 49% de las ocasiones cuando se encuentran por delante de
ella (ver Figura 2).
El
orificio primario en las fistulas de origen criptoglandular frecuentemente se
encuentra en la linea anorrectal en el origen de la glándula anal Para
facilitar su localización, en el quirófano y bajo anestesia, se puede aplicar
un poco de peróxido de hidrógeno diluido y pasarlo a través de un catéter que
se introduce por el orificio fistuloso secundario mientras se realiza la
anoscopia. El burbujeo del peróxido a través del orificio fistuloso primario
muestra su localización y la presencia de un trayecto.
Parks
realizó un estudio de 400 pacientes con fistulas de origen criptoglandular
clasificándolas en un trayecto en medio de ambos esfinteres y son las más
comunes; 2) transesfintéricas, el trayecto atraviesa el esfinter externo a
diferentes niveles. En este tipo la clasificación habitual es: un compromiso
mayor de 30%, se considera alta, y menor, baja; 3) supraesfintéricas, pasan
proximal a través del espacio interesfintérico antes de hacer un giro en U
sobre el músculo puborrectal y penetrar al elevador del ano, entrando a la fosa
isquiorrectal para salir por la piel perianal; 4) extraesfintérica, la más rara
de todas las fistulas, pasa directamente del recto a la piel perianal pasando
por fuera del complejo esfinteriano. Actualmente, se considera que este último
tipo de fistulas no necesariamente es de origen criptoglandular, y que tienen
una etiologia intraabdominal o por trauma.
Las
fistulas anales se deben clasificar con base en la relación entre el trayecto
fistuloso y los músculos del complejo esfinteriano.
La
continencia en pacientes operados por fistulas transesfintéricas y
supraesfintéricas a los cuales se les realizó manometría preoperatoria fue
mejor, en comparación con aquéllos en los cuales no se realizó. Es probable que
la manometría anorrectal preoperatoria pueda influenciar el resultado funcional
posterior a la cirugía guiando la utilización apropiado de una técnica
preservadora de esfínter.
La manometria debe ser utilizada en casos seleccionados cuando el paciente tiene antecedentes de incontinencia previa.
La fistulografía, el ultrasonido endoanal, la resonancia magnética y la tomografía computada son estudios que permiten definir la anatomía de la fistula anal.
La
fistulografía no está recomendada como estudio de primera elección para el
estudio del paciente con fistula anal.
La fistulografia tiene un rol limitado en el diagnóstico de la fistula anal, pero tiene su utilidad en las fistulas extraesfintéricas, particularmente cuando se sospecha su origen en un órgano intraabdominal o pélvico, así como un trayecto o extensión extraperineal (e.g. pared abdominal).
La
tomografia computada puede ser útil cuando la resonancia magnética no está
disponible o está contraindicada para detección de patología abdominal
asociada,
El ultrasonido, por su costo y beneficio, es el primer examen de diagnóstico para el estudio de una fistula anal.
La
ultrasonografia anal es el estudio de primera linea en el paciente en quien se
sospecha una fistula compleja.
La
sensibilidad y especificidad combinada de la resonancia magnética para la
detección de la fistula anal es de 87% y 69%, respectivamente, la cual se
compara y es muy similar a la del ultrasonido endoanal.
TRATAMIENTO
DE FISTULAS ANALES SIMPLES
La sección quirúrgica del esfínter anal externo e interno puede alterar la continencia fecal; esta alteración generalmente se presenta posterior al tratamiento de las fistulas complejas.
La
fistulectomia se asocia con mayor tiempo de curación, heridas más amplias,
mayor riesgo de incontinencia y la recurrencia es comparable con la
fistulotomia.
La fistulotomía es el tratamiento de elección para las fistulas simples, con una recurrencia de entre 2% y 9%, y con alteración en la continencia de 0% a 17%.
La marsupialización acorta el tiempo de cicatrización y el sangrado posoperatorio.
Se debe marsupializar los bordes de la fistulotomia,
Los
factores de riesgo identificados para alterar la continencia posterior a una
fistulotomía por una fistula interesfintérica son: pacientes con antecedentes
de cirugias de drenaje y la disminución de la presión de contracción en una
manometría.
En todos los pacientes programados para fistulotomía deberá realizarse un interrogatorio dirigido para detectar trastornos de "soiling". En aquellos que resulten con presencia de esta alteración, es necesario realizar una manometría.
En
todos los pacientes programados para fistulotomia deberá calcularse la escala
de Jorge Wexner (Cleveland Clinic) para valorar la continencia fecal. En
aquellos con puntaje diferente a 0, es necesario realizar una manometría.
Los pacientes con disminución de la presión de contracción deberán ser tratados con alguna técnica preservadora de esfínter.
La aplicación de colágena tiene una tasa baja de éxito en fístulas simples.
El
drenaje de un absceso perianal con fistulotomía primaria reduce el riesgo de
recurrencia de un absceso y persistencia de una fistula, y la necesidad de una
cirugía subsecuente.
Un número reducido de pacientes presenta incontinencia transitoria posterior al drenaje de un absceso con fistulotomía primaria, y la evidencia a largo plazo de persistir con incontinencia es débil.
La
fistulotomía primaria no se debe realizar en pacientes con abscesos con
fistulas altas o supraesfintéricas, o en los considerados como fistulas
complejas.
TRATAMIENTO DE FÍSTULAS ANALES
COMPLEJAS
Los
colgajos de avance endoanal pueden ser utilizados para el tratamiento de la
fístula compleja.
El
setón es un tubo que puede estar hecho de sutura de seda, látex, silastic,
entre otros, el cual se pasa a través del trayecto fistuloso primario para
convertir un proceso inflamatorio en una reacción a cuerpo extraño, con el fin
de provocar fibrosis periesfintérica. Los setones pueden clasificarse en: de
corte o de drenaje. Los setones de corte se ajustan en el consultorio a
intervalos de tiempo y los setones de drenaje se mantienen colocados por
intervalos variables de tiempo.
En las
fistulas anales complejas se puede utilizar el setón de drenaje como un puente
para realizar un procedimiento resolutivo posterior (e.g. avance de colgajo,
colocación de tapón, etc.), o convertirlo a un setón de corte. Las alteraciones
en la continencia se presentan en 0% a 54% de los casos cuando se utiliza setón
de corte.
En las fístulas anales complejas el tratamiento con setón es una opción.
La
utilización de tapón de colágeno o algún otro biomaterial para las fistulas y
el pegamento de fibrina son terapias para pacientes muy seleccionados se les
debe informar sobre la alta posibilidad de recidiva.
No hay evidencia científica suficiente para recomendar el uso rutinario de la técnica de LIFT, se utiliza en pacientes seleccionados.
El
tratamiento VAAFT sólo debe emplearse en casos muy seleccionados y realizados
por coloproctólogos calificados, ya que aún no hay evidencia de su eficacia a
largo plazo.
TRATAMIENTO DE LAS FÍSTULAS ANALES
SECUNDARIAS A ENFERMEDAD DE CROHN
Los
pacientes con fistulas anales y enfermedad de Crohn que se encuentran
asintomáticos no requieren de tratamiento quirúrgico.
La
fistulotomia en pacientes con enfermedad de Crohn muy seleccionados es segura y
efectiva siempre y cuando no involucre una porción muy importante del esfinter.
Previamente, en estos pacientes se deberá valorar la actividad de la enfermedad
anorrectal, la función del esfinter anal y la continencia, la complianza
rectal, la presencia de proctitis activa, cirugías anorrectales previas y la
consistencia de las evacuaciones. Posterior a la fistulotomía el rango de
cicatrización es de 56% a 100%, en un promedio de 3 a 6 meses.
Los pacientes con enfermedad de Crohn y fistulas sintomática muy bajas y simples pueden ser tratados con fistulotomia.
Las fistulas en enfermedad de Crohn deberán ser tratadas con setón de drenaje a largo plazo.
La
utilización de setón de drenaje con infliximab es otra opción de tratamiento.
En
pacientes en quienes no es posible controlar los síntomas ni la enfermedad
anorrectal fistulosa puede ser necesario un estoma permanente, o realizar una
proctectomía.
TRATAMIENTO DE LAS FISTULAS ANALES EN SITUACIONES ESPECIALES
Las
fístulas en herradura o hemiherradura son poco frecuentes y se definen como
aquéllas con una extensión circunferencial o hemicircunferencial que conectan
ambos lados o un solo lado de la región anorrectal a través del espacio
perianal, interesfintérico o, más común, isquiorrrectal. La cripta de origen es
habitualmente en línea media posterior y en 60% de los casos tienen extensión
al espacio postanal profundo.
La
fistula en herradura se debe tratar drenando el trayecto principal con un setón
de drenaje y simultáneamente una desbridación amplia de la fosa (s)
isquiorrectal(es) involucrada (s) con destechamiento de la colección principal
que habitualmente se localiza en el espacio post-anal profundo, dejando las
heridas abiertas.
En los
pacientes con VIH y fistula anal se deben descartar infecciones de transmisión
sexual asociadas, y considerar tomar biopsias bajo anestesia.
Los
pacientes con VIH en fase temprana, sobre todo quienes tienen adecuado
tratamiento antiviral, pueden ser tratados con fistulotomía convencional; aquéllos
con enfermedad avanzada, se deben tratar mínimamente con drenaje de los
abscesos con pequeñas incisiones o colocación de setón de drenaje.
La
cirugía de la fistula anal ha pasado por diferentes períodos históricos:
habilidades manuales, bases científicas y nuevas terapias biológicas en
desarrollo La experiencia del cirujano sigue siendo esencial para el
tratamiento de una fistula anal compleja.
Las
fistulas simples pueden ser tratadas por el cirujano general, dependiendo de su
experiencia, y de preferencia contando con el apoyo de un coloproctólogo, por
el especialista en coloproctología.
Todas
las fistulas complejas y recurrentes deberán ser tratadas por el cirujano
coloproctólogo.
Se
deberán referir a tercer nivel todas las fistulas específicas por Enfermedad de
Crohn o aquellos pacientes con fistulas complejas, si en su hospital de segundo
nivel no cuentan con los recursos diagnósticos o terapéuticos para su atención.
Las
guías más recientes de la Asociación Americana de Cardiología recomiendan la
utilización preoperatoria de antibióticos previos a la incisión y drenaje de
tejidos infectados en pacientes con válvulas protésicas, endocarditis
bacteriana previa, enfermedades cardíacas congénitas y trasplantados de corazón
con enfermedad cardiovascular.
No
existen ensayos clínicos controlados sobre la utilidad de los enemas o
preparación mecánica completa y antibióticos preoperatorios para mejorar la
recuperación o evitar complicaciones por el tratamiento de una fístula anal.
La
utilización de enemas y preparación mecánica preoperatoria, así como
antibióticos profilácticos y posoperatorios queda a consideración del cirujano,
de acuerdo a la técnica quirúrgica empleada. Se sugiere su utilización en caso
de planear una colocación de tapón de colágeno o una esfinteroplastia
concomitante al procedimiento de la fistula.



















No hay comentarios.:
Publicar un comentario