ACIDOSIS TUBULAR RENAL
La ATR
es una entidad clínica en la cual el paciente desarrolla una acidosis
metabólica debido a distintos trastornos en el túbulo renal. La acidosis
metabólica se refiere al mecanismo fisiopatogénico que da origen a la
disminución del bicarbonato sérico (HCO) con un pH menor de 7.4. Cuando los
mecanismos de compensación para mantener el pH en límites normales (7.35 a 7.4)
son ineficaces se presenta la acidosis metabólica descompensada.
La ATR
en niños está relacionada con defectos hereditarios, o adquiridos, que afectan
la habilidad del riñón para absorber HCO3, o excretar amonio o ácido. Esta
enfermedad fue descrita inicialmente en 1935 por Reginald Lightwood. Siendo
confirmada como un trastorno tubular renal en 1946 por Albright, que introdujo
el término de nefrocalcinosis, y en 1951, Pines y Mudge designaron el término
de acidosis tubular renal.
Con
base a criterios clínicos y fisiopatológicos la ATR se clasifica en:
Acidosis tubular renal distal (tipo 1)
Relacionada a un defecto en la acidificación urinaria distal con presencia de
un pH urinario o elevado (>5.5 en acidosis metabólica sistémica)
Acidosis tubular renal proximal (tipo 2) Producido por un defecto en la reabsorción del HCO3, filtrado. Puede presentarse como una entidad aislada o más frecuentemente asociada a otras anomalías tubulares (síndrome de Fanconi).
Acidosis tubular renal mixta (tipo 3)
Comparte
características de los tipo 1 y 2
Acidosis tubular renal hipercaliémica (tipo
4)
Relacionado con falla en la amoniogénesis Deficiencia o resistencia a la aldosterona (Cuadro 1)
Los
tipos más frecuentes en la edad pediátrica son los 1 y 2 (distal y proximal),
pero es posible encontrar los otros tipos de ATR.
La ATR
tipo 1 es resultado de la incapacidad de secretar la carga de ácido diaria. En
ausencia de tratamiento con soluciones alcalinizantes, la retención de iones
hidrógeno, de forma progresiva, lleva a una disminución de la concentración de
HCO plasmático.
La ATR
tipo 2 es causada por reducción de la capacidad reabsortiva de HCO, por el
túbulo proximal, resultando en una disminución del HCO, sérico. La ATR tipo 2
puede presentarse en su forma aislada, la cuál se presenta raramente o formando
parte del síndrome de Fanconi. La falla tubular relacionada al sindrome de
Fanconi es caracterizada por hipofosfatemia acompañada de hiperfosfaturia,
hiperuricosuria, glucosuria con glucosa sérica normal, aminoaciduria,
proteinuria tubular y acidosis tubular renal,
En la
ATR tipo 3, se encuentra una alteración genética de tipo autosómico recesivo
que afecta tanto de forma distal como proximal, ligado a una deficiencia de la
anhidrasa carbónica tipo II. Este tipo de ATR parece tener mayor relación a un
síndrome con calcificaciones cerebrales, llamado Guibaud Vainsel, y tiene
asociación con dismorfismo facial y pérdida auditiva conductiva.
El
hipoaldosteronismo, al que está relacionado la ATR tipo 4, tiene como
consecuencia una hipercaliemia característicamente asociada a acidosis
metabólica.
Debido
a la controversia que ha surgido de la hipótesis del sobrediagnóstico de la ATR
en niños en nuestro país, generada por la falta de homogeneidad de los
criterios diagnósticos y a la diversidad en los recursos en las diferentes
instituciones, aunado a los avances en el diagnóstico molecular de las formas genéticas
y a la existencia de variedades secundarias, e incompletas de ATR es necesaria
la realización de una guía de práctica clínica que permita a los pediatras,
gastroenterólogos pediatras, endocrinólogos pediatras y nefrólogos pediatras
estandarizar criterios y estudios diagnósticos para disminuir el riesgo de
complicaciones a largo plazo con la detección temprana y oportuna de todas las
variedades de ATR en el país.
La ATR
es una entidad clínica causada por un grupo de defectos en la reabsorción de
bicarbonato (HCO.) en el túbulo proximal o en la secreción de iones hidrogeno
(H) en el túbulo distal o ambos: se caracteriza por acidosis metabólica
hiperclorémica con brecha aniónica (BA) sérica normal y filtración glomerular
normal o ligeramente disminuida (en donde la acidosis es desproporcionada a la
disminución del filtrado glomerular), en ausencia de otro trastorno ácido-base.
Consideraciones
generales y etiología
Con base a criterios clínicos y fisiopatológicos la ATR se clasifica en:
- ATR distal o tipo 1
- ATR proximal o tipo 2
- ATR mixta o tipo 3 ATR hipercaliémica o tipo 4.
Considerando la etiologia de la ATR puede clasificarse en:
Primaria:
- Con defectos genéticos conocidos .
- Sin defectos genéticos conocidos
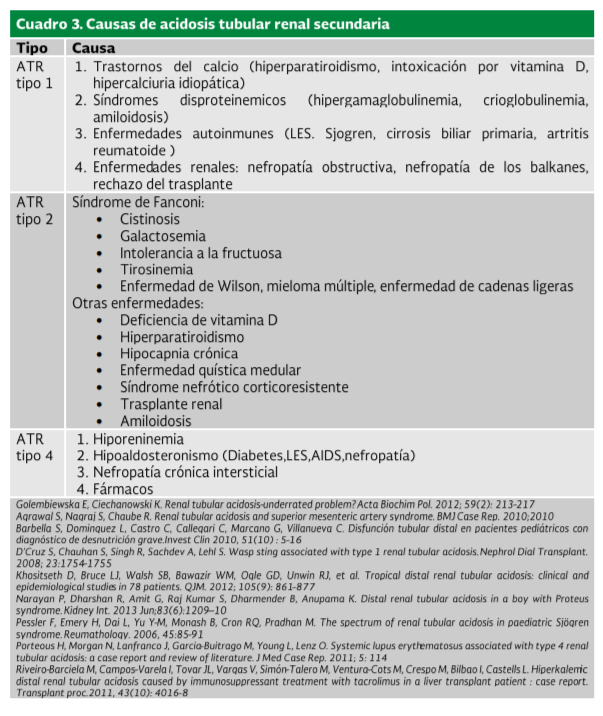
Secundaria:
- Medicamentos Tóxicos
Enfermedades:
- Genéticas Inmunológicas
- Renales
- Urológicos (malformaciones urinarias) Del metabolismo de calcio a Trasplanterenal
- (Cuadro 2 y 3)
Se sugiere que los pacientes, con enfermedades genéticas o adquiridas que presenten riesgo de presentar ATR sean valorados de forma intencionada en búsqueda de esta.
Existe relación de ATR tipo 1 con enfermedades autoinmunes, mas frecuentemente con el Sindrome de Sjörgren, con una prevalencia estimada hasta del 25%.
Otras enfermedades autoinmunes relacionadas con ATR tipo 1 son:
- Lupus eritematoso sistémico
- Hipergamaglobulinemia
- Cirrosis biliar primaria
- Tiroiditis autoinmune
- Hepatitis autoinmune
Una vez
establecido el diagnóstico de ATR se sugiere determinar la causa (primaria o
secundaria), asi como el sitio del defecto (proximal, distal o mixto).
La anfotericina B puede inducir ATR tipo 1 al incrementar la permeabilidad en el túbulo colector que favorece la caliuresis y la disminución de la secreción de H*, sin embargo, más frecuentemente se presenta diabetes insipida nefrogénica en combinación o no con ATR tipo 1. todo ello relacionado a la concentración intratubular de la anfotericina.
Se
sugiere considerar el diagnóstico de ATR tipo 1 en pacientes con antecedentes
de enfermedades autoinmunes descritas asi como con la administración de
medicamentos relacionados al riesgo de desarrollar este tipo de ATR.
La primera descripción de acidosis tubular renal Incompleta (ATR) fue hecha a partir del reporte de tres pacientes con nefrocalcinosis, pero sin hipercalciuria ni acidosis metabólica, hecha por Wrong y Davis en 1959.
La ATRI se caracteriza por:
Ausencia
de acidosis metabólica
Defecto
en la excreción renal de ácido
(demostrado por la incapacidad de reducir el pH urinario por debajo de
5.5, con la prueba de amonio o de
furosemide modificada)
La ATRi se caracteriza por los siguientes hallazgos clinicos. :
- Retraso en el crecimiento
- Raquitismo
- Nefrocalcinosis
- Bicarbonato sérico normal
- Hipercalciuria
- Hipocitraturia
En la ATRI, los efectos clínicos secundarios se limitan a:
- Nefrolitiasis
- Nefrocalcinosis
Se han reportado como causas frecuentes de ATR tipo 1 y ATRi las siguientes:
Niños
- Alteraciones urológicas:
- Valvas uretrales
- Reflujo vesicoureteral (RVU)
- Estenosis uretero-vesical
- Estenosis uretero piélica
- Vejiga neurogénica
Adultos
- Enfermedades autoinmunes
- Hiperparatiroidismo primario
EI RVU
es una de las alteraciones congénitas más frecuentes del tracto urinario,
ocurriendo en 1 de cada 250 recién nacidos vivos.
En caso
de contar con alteraciones urológicas, o alguna otra condición de riesgo para
presentar ATRI, se recomienda descartar daño tubular por medio de estudios
pertinentes, así como la corrección del defecto lo más pronto posible.
Se sugiere sospechar de ATRi en pacientes con talla baja, nefrocalcinosis, raquitismo, osteopenia, uropatía obstructiva o historia familiar positiva para ATR, asociados a gasometría normal.
Se
recomienda realizar pruebas de acidificación urinaria a todos los pacientes con
sospecha de ATRI, valorando de forma específica, la hiperamoniuria.
Debido a que se han observado tasas de crecimiento mayores en las niñas(os) que reciben corrección con HCO3, se recomienda, la administración de este en niños con ATRi posoperados de corrección de válvulas uretrales posteriores.
Hay
reportes anecdóticos que mencionan la presencia de acidosis tubular
transitoria, pero el grupo sugiere realizar más estudios para documentar o
descartar la presencia de acidosis tubular transitoria, ya que la evidencia
actual no es suficiente para realizar una conclusión.
Se
recomienda efectuar una historia clínica detallada, en búsqueda de causas
secundarias de ATR y en caso de encontrarse infección por VIH, efectuar los
estudios de laboratorio y gabinete pertinentes para confirmar o descartar ATR.
Las
siguientes son causas de ATR tipo 4, por la inhibición de reabsorción de sodio
en el túbulo colector por falla de voltaje negativo intraluminal:
- Deficiencia, resistencia o antagonismo de aldosterona
- Inhibición de renina
Medicamentos:
- Antiinflamatorios no esteroideos
- Heparina
- Inhibidores o bloqueadores receptores de angiotensina
- Diuréticos ahorradores de potasio Espironolactona
- Amiloride
- Triamterene
- Pentamidina
El
trimetroprim, comúnmente asociado con sulfametoxazol, puede interferir con la
función del canal de sodio epitelial, resultando en hipercaliemia y puede
interferir en las enzimas involucradas en la aminogénesis, provocando una
disminución de excreción de amonio que va acompañada de disminución de excreción
de hidrogenión, con presencia de ATR tipo 4 (hipercaliémica).
Se recomienda descartar acidosis tubular tipo IV en niñas(os) que reciban inhibidores de la enzima convertidora de angiotensina, antiinflamatorio no esteroideo, diurético ahorrador de potasio, timetroprim o pentamidina, que cursen con hipercaliemia y acidosis.
Se
sugiere el uso cauteloso de trimetroprim y sulfametoxazol en niños con factores
de riesgo para ATR.
DIAGNOSTICO
CLÍNICO
El signo predominante en la ATR es la detención del crecimiento, manifestado por disminución en la ganancia de peso y talla.
Dado
que el signo cardinal de la ATR es la talla baja, se sugiere realizar examen
clínico exhaustivo para encontrar más signos y síntomas de sospecha.
La
acidosis metabólica afecta en la acción de las siguientes hormonas:
- Hormona de crecimiento: supresión de la secreción
- Factor de crecimiento similar a la insulina tipo I (IGF-I): reducción de los niveles séricos
- Hormona tiroidea: depresión
- Glucocorticoides: Incremento de producción Paratohormona (PTH): Incremento de niveles
- Vitamina D: disminución de la activación
Se
habla de talla baja cuando ésta se sitúa por debajo de 2 desviaciones estándar
(DE), o bien por debajo del percentil 3, en las tablas correspondientes para la
edad y sexo o cuando la velocidad de crecimiento disminuye de forma sostenida,
es decir, inferior al percentil 25.
El
diagnóstico de talla baja debe de realizarse cuando el niño se encuentre 2 DE
por debajo de la edad, cuando existan registros por debajo del percentil 3 en la
tabla correspondiente para edad y sexo o cuando exista detención del
crecimiento.
La
talla baja puede ser un hallazgo aislado o el dato clínico de una gran variedad
de condiciones patológicas o trastornos heredados.
Se
recomienda realizar una exploración física exhaustiva para descartar
alteraciones físicas de otras enfermedades que causan alteraciones de
crecimiento, por ejemplo, síndrome de Turner.
La
correlación de la talla de la niña o del niño con la de sus padres es un
aspecto muy importante en la valoración del paciente con talla baja. El cálculo
de la talla blanco familiar permite valorar el
potencial
genético y sospechar una alteración del crecimiento cuando las predicciones de
talla se alejan de los valores esperados en forma persistente.
La
velocidad de crecimiento es el parámetro más valioso para evaluar el
crecimiento de la niña o el niño, al ser éste un proceso dinámico, una medición
aislada no tiene valor, ya que sólo determina la altura en ese momento. Se
seguirá esta evolución de la talla en la curva de velocidad de crecimiento que
recoge el valor absoluto de los incrementos en intervalos fijos de tiempo,
expresándose en cm/año.
Considerar,
al momento de la evaluación integral, la talla de los padres, y realizar
evaluación en seguimiento evitando realizar diagnóstico de talla baja con un
solo registro. Se sugiere sospechar ATR una vez descartadas las causas comunes
de detención de crecimiento.
Para un registro fidedigno de la talla se recomienda:
- En el niño <2 años de edad medir con un infantómetro
- En el niño >2 años de edad con un estadímetro
Para complementar el abordaje diagnóstico en niñas(os) con talla baja, el médico pediatra de segundo nivel de atención, deberá solicitar a niñas(os) con talla baja:
- Biometría hemática con diferencial
- Velocidad de sedimentación globular
Determinación sérica de:
- Urea
- Creatinina
- Gasometría venosa
- Cloro
- Sodio Potasio
- Calcio
- Fósforo
- Magnesio
- Transaminasas
- Fosfatasa alcalina
- Examen general de orina Coproparasitoscópico seriado
En el
abordaje del paciente con talla baja se requiere la toma de gasometría venosa,
en caso de documentarse talla baja con presencia de acidosis metabólica, se
sugiere realizar el protocolo de estudio para paciente con ATR.
Los
lactantes con ATR, como manifestación inicial, presentan fiebre sin causa
aparente, que se corrige con la reposición hídrica. De igual forma, pueden
presentar retraso en la dentición.
Los
pacientes con ATR pueden cursar con fluorosis y defectos en el esmalte dental.
Se
sugiere realizar una anamnesis extensa, así como una exploración física
exhaustiva, en todos los lactantes que presenten fiebre sin foco infeccioso
aparente, sobre todo en aquellos que presenten corrección del síndrome con
reposición hídrica y buscar de foma intencionada ATR.
Otros síntomas presentes en niñas(os) con ATR son:
- Poliuria
- Polidipsia
- Vómito
- Anorexia
- Constipación Deshidratación
- Hipotonía muscular
- Mialgias
- Fátiga
- Parálisis muscular severa
- Dolor óseo
- Deformidades óseas
- Raquitismo
Cuando se descartaron otras causas más comunes de peso y talla baja, se sugiere sospechar ATR cuando hay presencia de talla baja asociada con otras alteraciones tales como:
- Poliuria
- Polidipsia
- Deshidratación
- Nefrocalcinosis
- Sordera Raquitismo
- Hipotonía muscular
En la ATR, relacionada con patrón hereditario autosómico recesivo, se han reportado las siguientes anomalías en el desarrollo:
- Anormalidades oculares
- Glaucoma
- Catarata
- Queratopatía en banda
- Anormalidades auditivas
- Hipoacusia neurosensorial
- Sordera
- Calcificaciones cerebrales
- Retraso mental
La exploración física puede sugerir una alteración genética o malformación renal si existen alteraciones en:
- Pabellones auriculares
- Columna lumbosacra
- Genitales
- Hemihipotrofía fascio corporal
- Cara triangular
- Clinodactilia del quinto dedo
Debido
a que la ATR puede ser congénita o secundaria a otras patologías, se recomienda
realizar evaluación clínica completa y detallada, teniendo en cuenta las
alteraciones morfológicas relacionadas a ATR con patrón hereditario.
En
niños con ATR con patrón hereditario se sugiere buscar alteraciones oculares o
auditivas de forma intencionada
La ATR
induce manifestaciones sistémicas que incluyen hipercalciuria y
nefrocalcinosis. La hipocitraturia, presente en la ATR tipo 1, condiciona la
disminución de la solubilidad del calcio en la orina.
La
hipocitraturia, agregada a hipercalciuria y cambio de pH urinario hacia la
alcalinidad, condicionan un mayor riesgo de presentar nefrocalcinosis, la cual
es una complicación que se subdiagnostica, y por lo tanto, no tratada a tiempo.
Cuando
existen pH alcalinos urinarios (>7) se presentan depósitos de fosfato
cálcico, que facilitan la cristalización
Al ser
la nefrocalcinosis una complicación que amerita vigilancia estrecha, se
recomienda investigar la presencia de la misma, inmediatamente después de
realizar el diagnóstico de ATR.
Se
recomienda dar relevancia a los criterios clínicos sobre los hallazgos aislados
de laboratorio, teniendo en cuenta que se trata de un síndrome clínico.
Una vez sospechado el diagnóstico de ATR por datos clínicos y la presencia de acidosis metabólica hiperclorémica, con brecha aniónica normal, se sugiere solicitar los siguientes estudios:
- Gasometría venosa (segunda determinación)
- En suero: creatinina, ácido úrico, urea, albúmina, sodio, potasio, cloro, fósforo, calcio
- Examen general de orina y cuantificación en la misma de: creatinina, sodio, potasio, cloro, calcio
- Cálculo de brecha aniónica urinaria
- Cálculo de fracciones excretadas
- Pruebas de acidificación urinaria
GASOMETRIA
Parte
de las respuestas para compensar el desequilibrio ácido-base, están
determinadas por la concentración coordinada de HCO3 y PCO2, dependientes de la
respuesta respiratoria y renal, la cual comienza en la primera hora y se
completa en 12 ha 24 h.
La
albúmina constituye la mayor parte de aniones no medibles, por lo que la
reducción o incremento en la concentración de albúmina puede alterar la BA. La
BA disminuye 2.3 a 2.5mEq/l por cada gramo que disminuya la albúmina sérica,
mientras que aumenta a un grado similar con un incremento de la concentración
de albúmina.
En caso
de hipoalbuminemia, se sugiere corregir la BA, previa evaluación diagnóstica
integral.
Por
cada miliequivalente (mEq) que disminuye la concentración de HCO3 sérico, la
pCO2 arterial cae 1.2 mmHg.
Para realizar la evaluación correcta de acidosis metabólica, se sugiere hacer gasometría, BA y albúmina. Además de calcular la corrección respiratoria con la fórmula de Winter para poder clasificarla. (Cuadro 5)
La evaluación de cualquier desorden ácido-base debe comenzar con la medición de:
- pH
- PCO2
- Concentración de HCO3 (venosa o arterial)
- La concentración baja de HCO3 confirma la acidosis metabólica.
Se
recomienda realizar dos gasometrías venosas para fundamentar el diagnóstico de
acidosis metabólica, siendo la primera toma al momento de sospecha de ATR y la
segunda realizada por el nefrólogo pediatra para confirmación de los
resultados. (Cuadro 6)
La
PaCO, disminuye a medida que aumenta la altura sobre el nivel del mar por lo
que el HCO3 desciende, de 1 a 1.5 mmol/L por cada kilómetro de altitud.
Se
sugiere considerar la altitud del sitio donde se realizó la toma de muestra
para realizar los cálculos pertinentes y obtener la cifra de HCO3 sérico más
adecuada.
Los
pacientes con acidosis metabólica deben clasificarse dentro de 2 categorías
basados en la BA.
La BA distingue 2 tipos de acidosis metabólica:
Por pérdida o consumo de HCO3:
- ATR
- Diarrea
- Derivaciones urinarias ileostomías
Por acúmulo de ácidos orgánicos Insuficiencia renal crónica:
- Acidosis láctica
- Intoxicaciones
Se
recomienda clasificar a los pacientes con acidosis metabólica, de acuerdo a la
BA, teniendo en consideración que una característica de la ATR es presentar una
acidosis metabólica con BA normal, con pérdida o consumo de HCO3.
Existe
correlación entre los resultados obtenidos de gasometrías de muestras
arteriales y venosas, donde se encontró que el pH de sangre venosa es 0.04
menor, la pCO2 es 5.6 mmHg mayor y el HCO3 es 0.32 mmol/l mayor.(Cuadro 7)
Debido
a la relación entre muestras arteriales y venosas para gasometrías, se sugiere
realizar muestreo venoso, considerando la corrección pertinente.
La toma
de gasometría arterial conlleva mayor riesgo de complicaciones como: trombosis
arterial, lesión de nervios radial o ulnar, entre otras.
La
cuantificación de HCO3 obtenida por el análisis en gasometría venosa, presenta
rangos de valores superiores a los obtenidos por química sanguínea en autoanalizador, ya sea que la muestra se
guarde en hielo, con heparina o a temperatura ambiente. Esto aparenta estar
relacionado con buffers eritrocitarios, aunque el grupo de estudio fue pequeño,
y no se contó con estandarización de características de la población, que
permitan un análisis confiable.
No se
demostraron cambios significativos al almacenamiento de la muestra venosa para
análisis de HCO3 por química sanguínea de rutina, a las 0, 2 y 4 horas, ya sea
bajo temperatura ambiente, con uso de heparina o en hielo.
Es
recomendable utilizar gasometría venosa para la determinación de HCO3,
considerando los ajustes pertinentes de acuerdo a la edad y a la altura del
nivel del mar.
Para realizar el diagnóstico de acidosis metabólica se recomienda tomar como referencia los siguientes:
valores de HCO3 sérico por edad:
- < 2 años de edad: <18 mEq/l
- De 2 a 5 años de edad: <19 mEq/l
- >5 años: <20 mEq/l
Recomendamos efectuar diagnóstico de acidosis metabólica hiperclorémica por medio de gasometrías seriadas (2 tomas independientes).
La
determinación de CO2 por autoanalizador subestima el nivel de HCO3 en 3 a 6
mmol/l.
Se
sugiere no realizar únicamente determinación de CO2 total o pCO2 en sangre para
el diagnóstico de ATR.
Ya que
el nivel de HCO3 no se ve afectado con el ayuno, no es necesario suspender la
ingesta de alimentos previo a la toma de la muestra sanguínea.
QUÍMICA SANGUÍNEA
Electrolitos séricos
La
acidosis metabólica en ATR se encuentra acompañada de hipercloremia de forma
característica.
En
acidosis tubular renal el cloro sérico se encuentra característicamente elevado,
esto debido a mecanismos como defectos en el cotransportador HCO3/CI o
alteraciones en el eje renina - angiotensina-aldosterona.
El
sodio sérico habitualmente se encuentra normal, pero puede encontrarse
disminuido en casos de acidosis tubular renal tipo 4.
El potasio sérico aumenta en acidosis debido a la difusión del mismo al espacio intracelular, por intercambio con hidrógeno.(Cuadro 7).
El
fósforo sérico generalmente es normal pero está disminuido en casos de ATR tipo
2 secundaria a síndrome de Fanconi.
El
calcio habitualmente es normal, sin embargo puede estar bajo en casos de
deficiencia o resistencia de vitamina D.
En caso
de sospecha de ATR se debe realizar mediciones séricas de cloro, sodio,
potasio, calcio y fósforo, ya que se deben de documentar las alteraciones de
forma individual, además de ser necesarias para el cálculo de la brecha
aniónica.
Previa
verificación de que no existan patologías que causen acidosis metabólica
hiperclorémica como: diarrea crónica, presencia de ileostomía ureterosigmoidostomía,
se recomienda el abordaje con examenes de laboratorio para ATR en pacientes con
evidencia de talla baja, con o sin otros datos clínicos sugestivos, y realizar
el diagnóstico de ATR si existe la presencia simultánea de los cuatro parámetros
siguientes:
pH <7.37
HCO3:
- <18 mEq/l en < 2 años de edad
- <19 mEq/l de 2 a 5 años de edad
- <20 mEq/l en > 5 años de edad
- Brecha anionica sérica 8 a 16
- Cloro sérico > 110 mEq/l
CREATININA
La
creatinina habitualmente es normal, pero en nefritis instersticial o en
nefropatía obstructiva, que cursan con ATR secundaria, puede estar ligeramente
B elevada.
Para obtener los índices urinarios y las fracciones excretadas de HCO3 y fosfato, se requiere la cuantificación de creatinina en sangre y en orina, para el cálculo.
Realizar
cuantificación de creatinina para obtener las fracciones excretadas de HCO3 y
fosfato, teniendo en consideración que está se encuentra generalmente en
límites normales en ATR.
ANALISIS URINARIO
El pH
urinario puede ayudar a diferenciar el tipo de ATR en casi todos los casos:
>
ATR tipo 2:
- HCO; sérico bajo (sin tratamiento): pH <5.5
- HCO; sérico normal con tratamiento: pH >7
- y bicarbonaturia
ATR tipo 1:
- pH >6
- Independiente del HCO3 sérico
ATR tipo 4:
- pH <5.5 en acidosis
- pH >6 con HCO3 normal
En el
sedimento urinario de los pacientes con ATR se pueden encontrar cristales de
oxalato o fosfato cálcico en caso de existir hipercalciuria.
La densidad urinaria puede estar disminuida en casos de ATR secundaria a:
- Nefritis intersticial
- Nefropatía obstructiva
- Algunas causas de síndrome de Fanconi
La
determinacion urinaria de HCO3, Na, K, CI, Ca, y creatinina debe efectuarse en
muestra de orina fresca matutina, con mediciones simultáneas de los mismos
analitos en sangre o suero, determinando la fracción excretada de HCO3.
El Ca
urinario se determina con el fin de valorar si existe hipercalciuria, la cual
se observa frecuentemente en la ATR tipo 1, y es causa de E nefrocalcinosis.
Se
utiliza la relación calcio/creatinina (Ca/Cr), que es un índice que se obtiene
dividiendo la concentración urinaria de Ca en mg/dl, sobre la concentración
urinaria de creatinina en mg/dl.
El
límite superior normal es en:
- O a 6 meses: >0.8
- 7 a 11 meses: >0.6
- 1 a 2 años: >0.47
- 2 años: >0.21
- Preescolares de 0.3
- Adultos y escolares de 0.2
En
niños mayores de 1 año de edad, en recolección de orina de 24 horas, se
considera hipercalciuria valores mayores de 4 mg/kg/día.
En
niños con ATR tipo 1 se sugiere realizar valoración del índice
calcio/creatinina de forma semestral en presencia de nefrocalcinosis.
El
valor normal esperado de la eliminación urinaria de bicarbonato es menor al 2%.
Para clasificar la ATR, es necesario calcular la eliminación urinaria de
bicarbonato. (Cuadro 10)
Los valores de la fracción excretada de HCO3 urinario variarán de acuerdo al tipo ATR. Para poder clasificarla son:
ATR tipos 1 y 4: valores < 5%
ATR
tipo 2:
- Con administración de HCO3 y HCO3 sérico normal, valores >10%
- Sin administración de HCO3, valores <5%
ATR tipo 3: valores >5%
Para el
diagnóstico de ATR tipo 2, se realiza la prueba de fracción excretada de HCO3,
la cual requiere de la administración de HCO3 para lograr niveles séricos de
HCO3 de 20 a 22 mEq/l, si la fracción excretada es mayor de 10%, se confirma el
diagnóstico.
En
pacientes con acidosis metabólica aumenta la excreción de amonio acompañada de
aumento en el cloro urinario, por lo que es necesario calcular la brecha
anionica urinaria (BA) para determinar, en forma indirecta, la concentración de
amonio. En casos de acidosis tubular tipo 4, no hay suficiente producción de
amonio y el cloro urinario es bajo; de tal forma que cuando la brecha aniónica
urinaria presenta valor negativo, existirá una excreción suficiente de amonio y
lo contrario cuando tiene un valor positivo.
En
sospecha de ATR, se sugiere realizar el cálculo de la BAU, en presencia de
acidosis metabólica hiperclorémica.
En
cuanto a los electrolitos urinarios, con ATR tipo 1 la excreción urinaria de
sodio y potasio se encuentran elevadas, y para ATR tipo 4 la eliminación
urinaria de potasio disminuye y se eleva la de sodio.
En
presencia de hipocaliemia, un potasio urinario mayor de 20, o una fracción
excretada mayor de 40%, indica pérdidas renales de potasio las cuales se
observan en ATR tipo 1, tipo 3 y frecuentemente en tipo 2, en cambio, en
presencia de hipercaliemia, un potasio
urinario menor de 20, o una fracción excretada de potasio menor de 10%, indica
retención urinaria de potasio, lo cual se encuentra en ATR tipo 4.
Se habla de hipocitraturia cuando el índice citrato/creatinina es <400 mg/g o cuando en la recolección de orina de 24 horas se obtengan cifras <8 mg/kg/día.
En
pacientes con sospecha de ATR tipo 1 se sugiere evaluar los niveles de citrato
en orina
ULTRASONOGRAFIA
El diagnóstico de ATR debe incluir ultrasonido renal para detectar calcificaciones renales, litos renales, e investigar causas secundarias como uropatía obstructiva, nefropatía por reflujo y nefritis túbulo intersticial crónica. También es útil para llevar el seguimiento de nefrocalcinosis.
La nefrocalcinosis identificada durante las primeras semanas de vida, es irreversible.
La
nefropatía intersticial grave secundaria a nefrocalcinosis puede preceder a una
insuficiencia renal crónica poliúrica, complicación rara observada en 1 de cada
18 casos de ATR tipo 1 diagnosticado durante la infancia (en seguimiento de 2 a
18.5 años).
En todo
paciente con ATR se recomienda descartar la presencia o desarrollo de nefrocalcinosis
con ultrasonografía, a partir del momento diagnóstico. Así mismo, evidenciar
secundarias como uropatía obstructiva, n por reflujo, entre otras.
Pruebas de acidificación
urinaria
Las pruebas de acidificación urinaria permiten identificar el defecto característico en la ATR tipo 1.
Las pruebas de acidificación urinaria están indicadas en casos cuyo diagnóstico está en duda, y en donde los valores de HCO3 y cloro se encuentren limítrofes y existan datos clínicos de sospecha de acidosis tubular renal.
En
pacientes con HCO3 limítrofe o con duda diagnóstica, se deberá realizar pruebas
confirmatorias, como prueba de acidificación urinaria por el nefrólogo pediatra.
(Cuadro 6)
Con las
pruebas de acidificación urinaria se valora el pH urinario así como la
excreción urinaria de iones H+ (amonio y acidez titulable) a través de
diferentes estímulos:
- Furosemide
- Furosemide más fludrocortisona
- Acetazolamida
- Cloruro de amonio
Prueba con Furosemida y Furosemida con fludrocortisona:
El pH urinario menor a 5.32 descarta acidosis tubular renal distal
Medición de pCO2 urinaria máxima (prueba con infusión de HCO3, acetazolamida o ambas):
El
valor normal para la pCO2 urinaria máxima se considerara >60 a 70 mm Hg, con
un gradiente pCO2 orina-plasma >20 a 30 mmHg, valores por debajo de estos,
apoyan G el diagnóstico de ATR distal.
La
prueba de furosemide con fludrocotisona posee ciertas ventajas sobre la prueba
de cloruro de amonio ya que tiene la misma efectividad para identificar a los pacientes con ATR tipo 1 que no
acidifican orina, además que posee menos efectos adversos, siendo muy
importante esta consideración, ya que los pacientes abandonan la prueba de acidificación
por cloruro de amonio, por la presencia sea o vómito. Además, aparenta ser que,
la prueba de furosemide con fludrocortisona, se puede finalizar en menos tiempo
(90% de los pacientes sometidos a esta prueba tuvieron pH<5.3 a las 3 horas
o menos).
Para confirmar el diagnóstico de ATR tipo 1, las pruebas de furosemide у furosemide con fludrocortisona son muy sensibles pero poco específicas. De éstas, la prueba de furosemide con fludrocortisona da menos falsos positivos, pero en este momento la fludrocortisona no se encuentra disponible en México, aunque por su simplicidad se recomienda como primera prueba. De presentarse pH urinario menor de 5.3 se sugiere descartar ATR distal. Si el pH urinario es igual o mayor de 5.3 se recomienda realizar, como prueba confirmatoria, la PCO2 urinaria máxima.
En pacientes con sospecha de ATRi, realizar pruebas de acidificación urinaria.
En
pacientes con sospecha de ATR con ausencia de acidosis metabólica con pH
urinario alcalino y síntomas clínicos relacionados a ATR, se recomienda
realizar pruebas de acidificación urinaria para confirmar o descartar la
sospecha diagnóstica.
Se
sugiere realizar ultrasonido renal de forma anual en ATR tipo 1.
Las complicaciones de la ATR se deben principalmente al retraso en el diagnóstico y del tratamiento, e incluyen:
- Retraso del crecimiento
- Nefrocalcinosis
- Litiasis
- Dolor óseo
- Raquitismo
- Osteomalacia
- Osteoporosis
En casos graves pueden presentarse fracturas patológicas.
Agregado a la acidosis metabólica sistémica crónica, los siguientes factores presentes en ATR contribuyen al retraso en el crecimiento y desarrollo:
- Emesis frecuente
- Diarrea crónica
- Hipocaliemia
- Hipotonía muscular
- Anorexia
En pacientes con ATR tipo 1 se han reportado las siguientes complicaciones:
- Nefrocalcinosis
- Parálisis hipocaliémica
- Enfermedad renal crónica
- Hipercalciuria
Recientemente
se ha reportado alta prevalencia de osteoporosis en adultos con ATR tipo 1.
Para
evitar complicaciones, se sugiere realizar un diagnósico oportuno e iniciar
tratamiento de forma inmediata y mantener niveles de HCO3 adecuados, con
soluciones alcalinizantes, al tener el diagnóstico de ATR.
GENERALIDADES
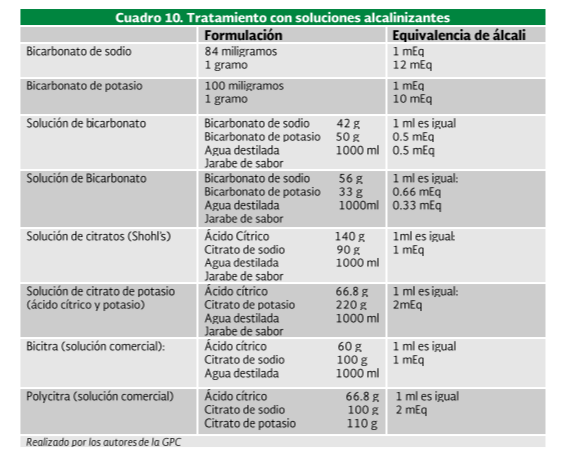
Cuando se corrobora el diagnóstico de acidosis tubular renal, el tratamiento inicial se realiza con soluciones alcalinizantes a dosis de 1 a 7 D mEq/kg/día.(Cuadro 10)
La
dosis habitual requerida de HCO3, de acuerdo al tipo de acidosis tubular renal,
es:
ATR tipo 1: 3 a 5 mEq/kg/día
ATR tipo 2: 10 a 15 mEq/kg/día
La cantidad de HCO3 requerida típicamente disminuye con la edad:
- Lactantes 5 a 8mEq/kg/día
- Niños 3 a 4 mEq/kg/día
- Adultos de 1 a 2 mEq/kg/día
Se
recomienda usar HCO3 de sodio o potasio a dosis inicial de 1 a 2 mEq/kg/día e
ir aumentando paulatinamente hasta llegar a niveles de HCO3 sérico >20 mEq/l
en niños de <2 años de edad y >22 mEq/I en niños >2 años de edad.
En la ATR tipo 2 se incrementa la dosis progresivamente hasta 14 mEq/kg/día, debido a las altas pérdidas de HCO3 en el túbulo proximal.
El
tratamiento para la ATR tipo 4 la dosis de HCO3 utilizada va de 1.5 a 2
mEq/kg/día.
En pacientes con ATR tipo 1 con hipocaliemia, la corrección del nivel de potasio se realizó con dosis de citrato de potasio en 4 mEq/kg/día. La administración del citrato de potasio reduce de forma significativa la excreción urinaria de calcio y fostato, con lo cual la producción de litos se ve reducida.
Se
recomienda utilizar solución de citratos en pacientes con ATR tipo 1,
preferentemente citrato de potasio, en presencia de hipercalciuria o Domro
hipocitraturia.
La meta a alcanzar en el tratamiento, de la acidosis tubular renal, con soluciones alcalinizantes, de acuerdo a edad, es:
0 a 2
años: >20 mEq/l
>2 años: >22 mEq/l
Se
sugiere mantener los niveles de HCO3 en 22 mEq/l para asegurar crecimiento y
evitar complicaciones.
El HCO3 puede mezclarse con jugos o bebidas saborizadas para mejorar el sabor y tolerancia oral.
En caso de documentarse ATR con nefrocalcinosis, se recomienda dar solución de citrato de potasio.
el
tratamiento incluye cápsulas o solución de fosfatos, acompañado de calcitriol.
Se
sugiere no suspender el tratamiento de forma súbita, en niños menores de 2 años
con datos clínicos francos de ATR, y mantenerse en hospitalización para
realización de pruebas diagnósticas confirmatorias.
En
niños con diagnóstico de acidosis tubular renal se debe vigilar el estado
hídrico y los niveles séricos de potasio.
Durante
el tratamiento de la ATR tipo 2, la bicarbonaturia produce pérdidas de sodio y
potasio.
Para
evitar hiponatremia e hipocaliemia, en la ATR tipo 2, se sugiere administrar
una mezcla de HCO3 de potasio y sodio.
De
integrarse el síndrome de Fanconi, además de administrar solución
alcalinizante, se recomienda que el tratamiento incluya cápsulas o solución de
fosfatos, acompañado de calcitriol.
Se sugiere no suspender el tratamiento de forma súbita, en niños menores de 2 años con datos clínicos francos de ATR, y mantenerse en hospitalización para realización de pruebas diagnósticas confirmatorias.
En niños
con diagnóstico de acidosis tubular renal se debe vigilar el estado hídrico y
los niveles séricos de potasio.
Se han
reportado ciertas consecuencias por el uso de HCO3 entre las que se han
destacado por vía oral:
- Dispepsia
- Intravenoso:
- Trastornos electrolíticos: hipocaliemia,
- hipocloremia, hipocalcemia, hipernatremia Alcalosis metabólica
- Efectos respiratorios: hipercapnia con apnea
- Efectos cardiacos: disminución en la contractilidad cardiaca, prolongación del intervalo QT y arritmias ventriculares
- Efectos neurológicos: parestesias, contractura muscular, tetania, mioclonus (probablemente secundaria a hipocalcemia), crisis convulsivas
Al administrar HCO3 de sodio se recomienda vigilar el desarrollo de los siguientes, como posibles complicaciones por su administración:
- Alcalosis metabólica
- Hipocaliemia
- Arritmias
- Parestesias
- Úlcera gastroduodenal
- Hipercaliemia Infección urinaria
- Deterioro de la funcion renal
Al administrar
citratos, se debe vigilar la aparición de distensión abdominal, diarrea,
hipercaliemia.
Los
citratos no se recomiendan en casos de hipercaliemia, infección urinaria,
deterioro de la función renal, así como en aquellos pacientes que se encuentren
bajo uso de diuréticos ahorradores de potasio, amiloride o inhibidores de la
enzima convertidora de angiotensina.



























No hay comentarios.:
Publicar un comentario