ADENOCARCINOMA GASTRICO
El
cáncer de estómago o cáncer gástrico es un tipo de crecimiento tisular maligno
producido por la proliferación contigua de células anormales con capacidad de
invasión y destrucción de otros tejidos y
órganos, en particular el esófago y el intestino delgado.
En las
formas metastásicas, las células tumorales pueden infiltrar los vasos
linfáticos de los tejidos, diseminarse a los ganglios linfáticos y,
sobrepasando esta barrera, penetrar en la circulación sanguínea para
diseminarse a cualquier órgano del cuerpo.
El
cáncer gástrico, es un padecimiento que suele presentarse en forma asintomática
en las etapas iníciales, al momento del diagnóstico, aproximadamente el 50 % de
los pacientes presentan una etapa loco regionalmente avanzada y de las etapas
tempranas resecadas tienen metástasis a ganglios linfáticos regionales entre el
70 y el 80%.
El
cáncer gástrico se reporta como la segunda causa de muerte a nivel mundial con
aproximadamente 600,000 muertes al año; situación que se genera en parte por el
envejecimiento y crecimiento de la población (cerca del 90% de los pacientes
que lo presentan, son mayores de 50 años). Se ha estimado que para el 2010,
habrá 1.1 millón de casos nuevos, lo que representará una importante carga a
los sistemas de salud, sobre todo en los países en desarrollo.
Un
estudio retrospectivo realizado en nuestro país reportó que el 80.2% de los
pacientes con esta neoplasia se diagnosticaron en etapa IIIB y IV;
La
mayor parte de los tumores malignos de estomago son adenocarcinomas. Desde el
punto de vista histológico, los adenocarcinomas se han clasificado en dos
subtipos: intestinal y difuso; aunque algunos tumores no pueden ser
clasificados en alguno de estos subtipos y otros presentan características
histológicas de ambos. También los adenocarcinomas de estómago pueden ser
clasificados por el sitio anatómico de origen: proximales sí surgen en la
región del cardias gástrico o dístales, si surgen en cualquier otro sitio.
La enfermedad
en etapas tempranas es habitualmente asintomática, mientras que la dispepsia y
los datos clínicos de alarma (pérdida de peso, masa abdominal palpable,
disfagia, hemorragia del tubo digestivo alto, anemia y/ó vomito persistente) se
presentan en etapas avanzadas de la enfermedad.
En la actualidad se sabe que la sobrevida global es de 3 a 4 meses sin tratamiento y de 8 a 11 meses con quimioterapia, a diferencia de la etapa temprana que alcanza una sobrevida de 30 a 40 % a 5 años con tratamiento multimodal.
La edad
mayor a 55 años y el sexo masculino, son factores de riesgo para presentar
cáncer gástrico.
Se
recomienda una vigilancia estrecha de pacientes masculinos con más de 55 años y
tabaquismo importante, que presenten datos clínicos de dispepsia de inicio
reciente.
Se
recomienda el consumo de frutas y vegetales frescos que contengan vitamina C.
No se
recomienda el uso de suplementos con antioxidantes para reducir el riesgo de
cáncer gástrico.
Estudios
de casos y controles han mostrado una asociación positiva entre la ingesta de
sal y nitratos/nitritos (alimentos ahumados) con el cáncer gástrico.
Se
recomienda evitar o suspender el uso del tabaco.
Pruebas
de detección específica o factores de riesgo
La
infección con H. pylori, aumenta al doble el riesgo para desarrollar cáncer
gástrico.
Los
pacientes con infección con H. pylori, gastritis atrófica severa, gastritis
predominante en el cuerpo del estomago y/o metaplasia intestinal tienen mayor riesgo
de desarrollar cáncer gástrico.
Se recomienda la erradicación de H. pylori, en pacientes que tienen cáncer gástrico y en aquellos con riesgo alto para desarrollarlo.
En nuestro medio no se recomienda la búsqueda y tratamiento de H. pylori, como tamizaje para reducir el riesgo de cáncer gástrico.
Los
pacientes que presentan alguno de los siguientes síndromes: poliposis
adenomatosa familiar, cáncer de colon no-poliposis hereditario y el síndrome de
Peutz-Jeghers; tienen mayor riesgo para desarrollar cáncer gástrico.
Ofrecer
consejo genético a los pacientes que presenten los síndromes antes mencionados.
Las mutaciones del gen de la cadherina E, condicionan un riesgo del 75 – 85 % de desarrollar cáncer gástrico.
Los pacientes que cumplan criterios de Ámsterdam (ver definición) para cáncer gástrico difuso hereditario deberán de recibir consejo genético y considerar la gastrectomía profiláctica.
DIAGNOSTICO CLINICO.
Los pacientes con cáncer gástrico, en etapas tempranas pueden cursar asintomáticos. En etapas avanzadas la sintomatología puede ser: náusea, saciedad temprana, vómitos persistentes, sangrado y anemia.
Los
siguientes datos clínicos son predictores de cáncer gástrico:
- Disfagia OR 3.1
- Pérdida de peso OR 2.6
- Edad > 55 años OR 9.5
- Dispepsia no complicada a cualquier edad, es un predictor negativo de cáncer OR 0.1
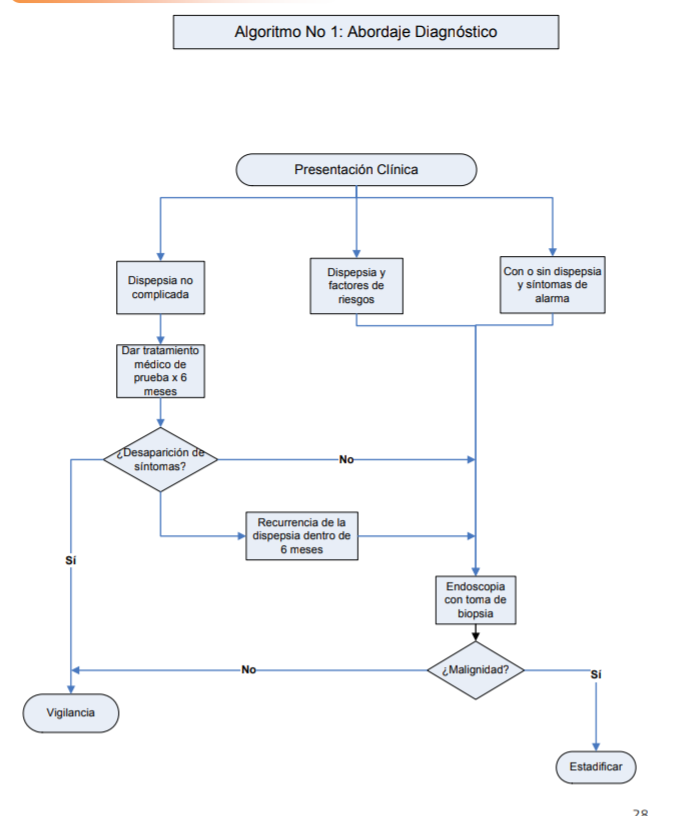
A los pacientes con datos de dispepsia no complicada, se les puede ofrecer inicialmente un tratamiento médico de prueba por 6 meses.
Pacientes con datos de dispepsia no complicada y tratamiento médico, que no presenten mejoría a los 6 meses o que presenten recurrencia de la dispepsia, se les debe realizar endoscopia.
Pacientes con o sin dispepsia y cualquier síntoma de alarma (disfagia, pérdida de peso, anorexia, vomito recurrente, sangrado digestivo) independientemente de la edad, se le debe realizar endoscopia.
A los
pacientes con edad > 55 años y dispepsia no complicada, se les debe realizar
endoscopia para descartar cáncer gástrico.
El número de síntomas de alarma en pacientes con cáncer gástrico, correlaciona con el estadio del tumor: a mayor número de síntomas de alarma, estadio más avanzado de la enfermedad.
En pacientes con cáncer gástrico, la duración de los síntomas, no se relaciona con peor pronóstico.
Investigue
la presencia de síntomas de alarma en los pacientes con dispepsia, para
descartar datos que sugieran diagnóstico de cáncer gástrico.
Pruebas Diagnósticas
La
endoscopia gastrointestinal alta, tiene una sensibilidad de 90 % para el
diagnóstico de cáncer gástrico, permite la toma de biopsia y evita el uso de
radiación ionizante.
Se recomienda la endoscopia flexible gastrointestinal alta con toma de biopsia, como el procedimiento de elección para el diagnóstico en pacientes con sospecha de cáncer gástrico.
El uso de tinciones (Lugol, carmín índigo) durante la endoscopia, puede mejorar la detección de lesiones pequeñas o pre malignas.
No se
recomienda de forma rutinaria el uso de tinciones durante la endoscopia, pero
puede ser de valor en pacientes seleccionados.
Diagnóstico histológico
La
exactitud en el diagnóstico de malignidad, aumenta con el número de biopsias
tomadas.
Para
cáncer gástrico, se recomienda tomar un mínimo de 3 biopsias.
El diagnóstico de malignidad, debe ser corroborado por un patólogo con experiencia en patología gastrointestinal.
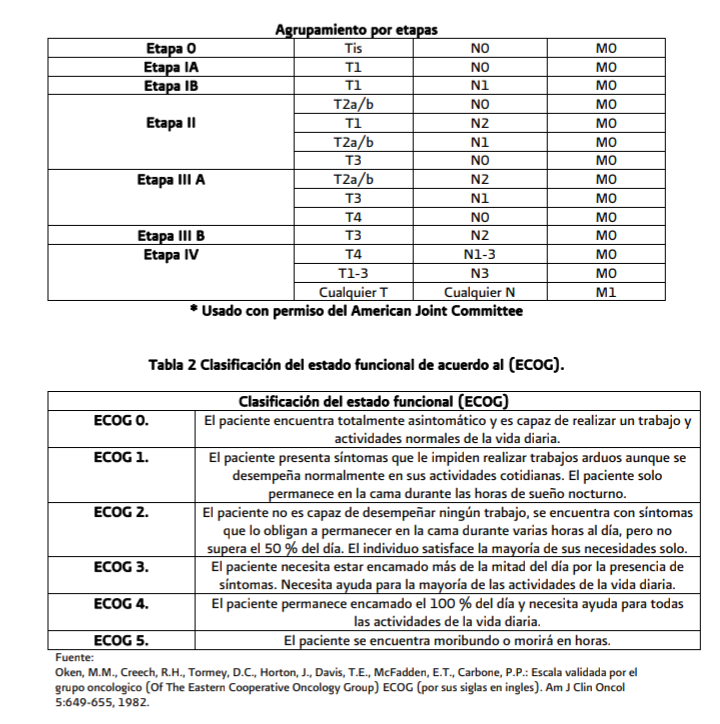
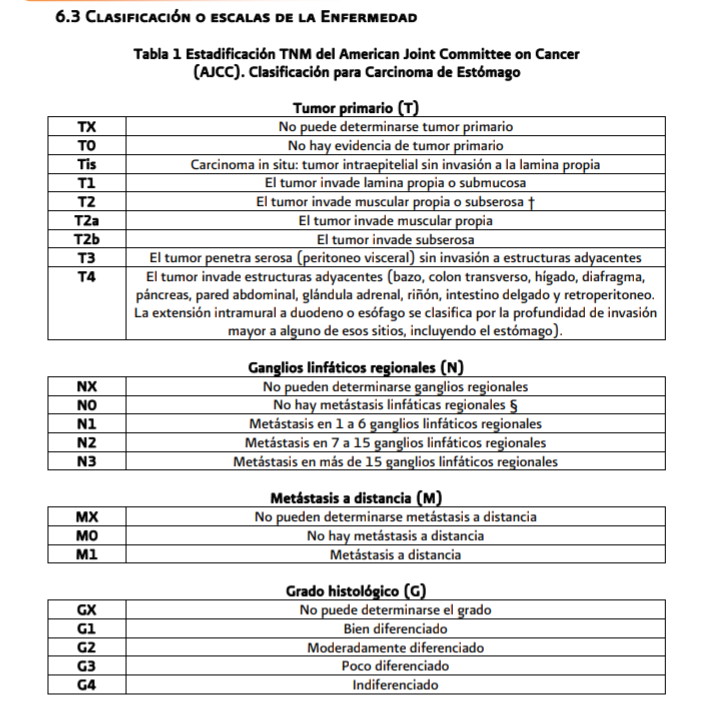
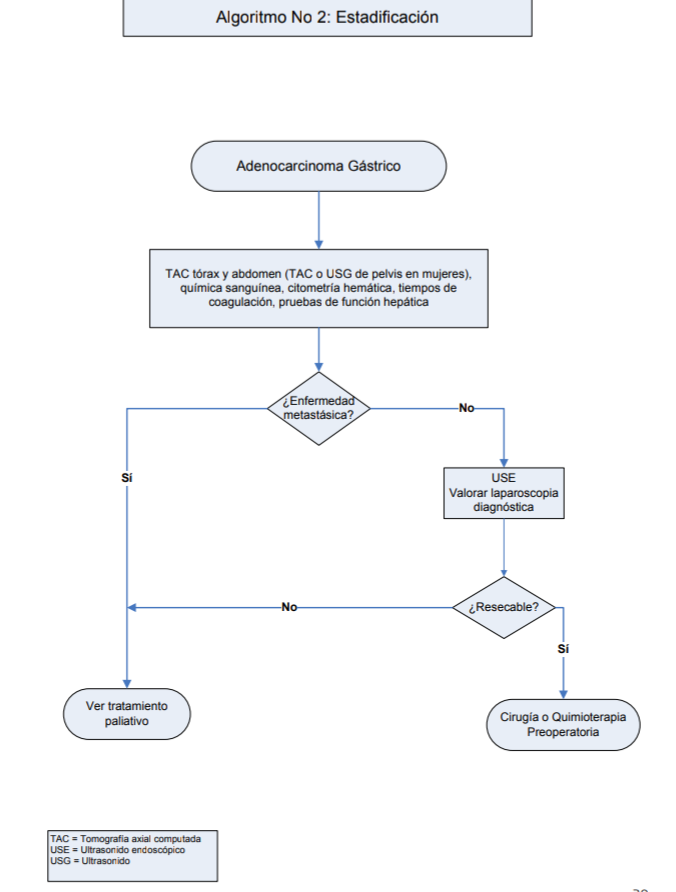
Estadificación (ver tabla 1 de
anexo 6.3 y algoritmo 2)
La
tomografía computarizada (TAC) con medio de contraste es el método no invasivo
más exacto (sensibilidad de hasta 78% y especificidad de 92%) para detectar metástasis a distancia.
La tomografía con emisión de positrones (TEP), tiene una especificidad mayor (92%) y una sensibilidad menor (56%) que la TAC para la detección de ganglios linfáticos positivos.
Para la estadificación, se recomienda realizar en forma rutinaria, TAC de tórax y abdomen con contraste intravenoso y distensión gástrica con medio de contraste oral o agua.
No se
recomienda el uso rutinario de TEP, para realizar la estadificación
preoperatoria.
A los pacientes a quienes se les realiza el diagnóstico de cáncer gástrico por primera
ocasión, se deberá de realizar con fines de estadificación (ver Anexo 6.3 Tabla 1):
historia clínica y examen físico completos así como endoscopia completa del tracto gastrointestinal alto, citometría hemática completa, química sanguínea, tiempos de coagulación, pruebas de función hepática, TAC torácica, TAC abdominal, TAC o USG de pelvis en las mujeres y prueba de detección de H. pylori
El ultrasonido endoscópico (USE), ha demostrado ser superior a la TAC en dos estudios prospectivos cegados, para establecer el T (profundidad del tumor) y N (estado ganglionar).
El USE
tiene una sensibilidad para establecer el T que va del 77.8 % al 100 % y una
especificidad de 57.9 al 100 %.
Se recomienda el USE en todos los pacientes con cáncer gástrico y de la unión esófago-gástrica que sean candidatos a un tratamiento curativo.
La laparoscopia tiene una sensibilidad del 88 % y una especificidad del 100 % para establecer resecabilidad.
Sólo se
recomienda la laparoscopia sí el tumor gástrico es considerado para tratamiento
quirúrgico inicial.
La RM
sólo deberá emplearse en pacientes a los que no sea posible realizar la TAC o
como estudio adicional a la TAC/USE.
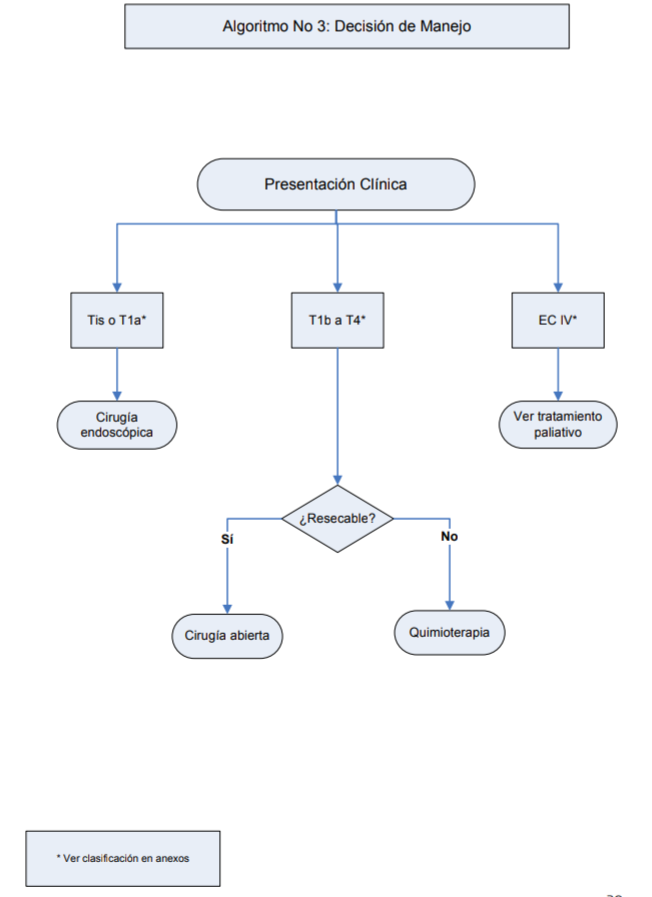
TRATAMIENTO
FARMACOLOGICO
La quimioterapia perioperatoria con ECF se debe de emplear en los pacientes con adenocarcinoma gástrico ≥ T2 considerados resecables.
No hay esquema de quimioterapia estándar de segunda línea.
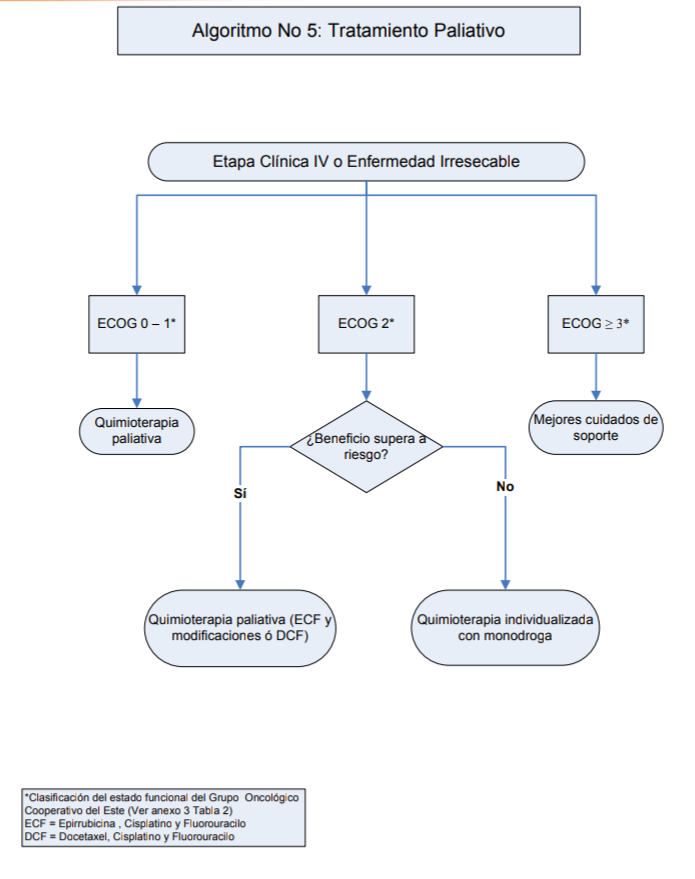
Se
recomienda la quimioterapia paliativa en los pacientes con estado funcional
(ECOG, ver Anexo 6.3 Tabla 2) ≤ 2, mientras que los pacientes con ECOG ≥ 3 se
deberán tratar con mejores cuidados de soporte.
Se recomienda la quimioterapia con triple agente (epirrubicina o docetaxel, cisplatino y fluorouracilo) en pacientes con etapa avanzada y estado funcional de 0 ó 1.
Se deberá de valorar riesgo beneficio del emplear quimioterapia de combinación en pacientes con etapa avanzada y estado funcional de 2.
El capecitabine y oxaliplatino podrán suplir al fluorouracilo y cisplatino respectivamente en el esquema de ECF.
No se recomienda un tratamiento de quimioterapia de segunda línea como estándar.
El uso de palonosetron asociado a dexametasona es superior en control de la nausea aguda y tardía en comparación con ondasentron.
Se recomienda el uso de dexametasona mas ondasentron para el control de nausea asociada a quimioterapia.
Palonosetron
se recomienda para esquemas con potencial alto de emesis tardia.
Se
requiere mayor evidencia para recomendar como tratamiento estándar el herceptin
asociado a quimioterapia en primera línea en cáncer gástrico avanzado.
TRATAMIENTO
QUIRURGICO
La resección endoscópica de la mucosa (REM) es un tratamiento seguro para el adenocarcinoma in situ de estomago.
Se recomienda realizar mucosectomía endoscópica, cuando el médico endoscopista cuente con la experiencia suficiente en el procedimiento y en lesiones menores de 30 mm.
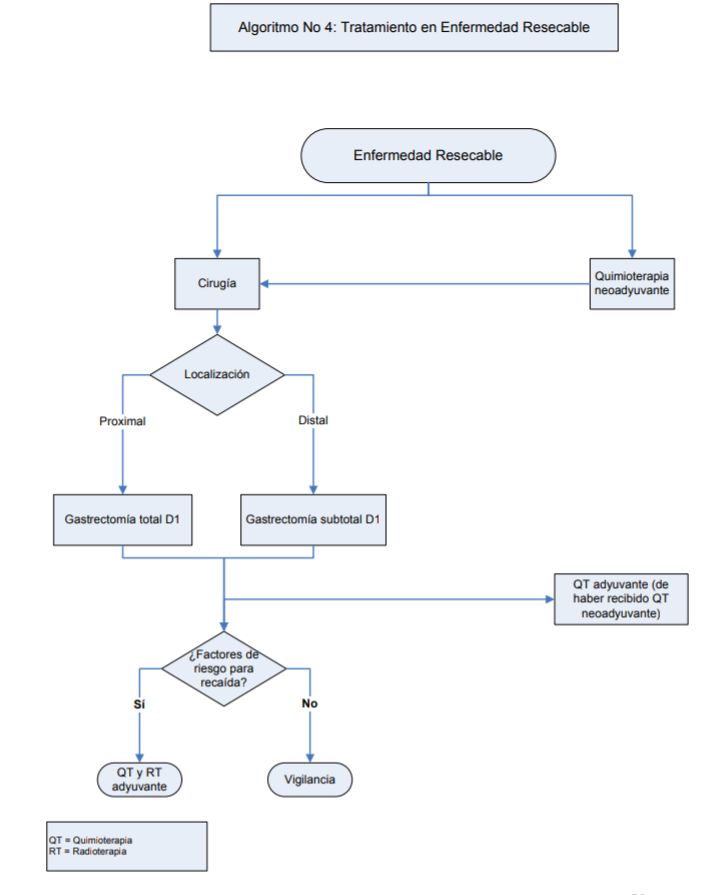
El tratamiento efectivo para el adenocarcinoma gástrico es la cirugía y el tiempo de sobrevida luego de la resección está directamente relacionado con la etapa del tumor.
Se recomienda realizar cirugía en aquellos pacientes potencialmente resecables independiente de la EC, incluidos aquellos pacientes que recibieron QT neoadyuvante.
La
cirugía para el adenocarcinoma gástrico debe tener como objetivo principal
obtener una resección completa (RO) con márgenes adecuados.
La
cirugía se debe considerar como prioridad quirúrgica alta, para ser resuelto en
un servicio oncología quirúrgico.
La cirugía paliativa debe ser considerada en aquellos pacientes con enfermedad avanzada pero sin carcinomatosis peritoneal.
Los bypass o stents gástricos pueden ser alternativas dentro de los cuidados paliativos del adenocarcinoma gástrico.
En la
actualidad no se recomienda en forma general realizar disecciones D2, aunque
existe evidencia de un pequeño grupo de pacientes que se beneficiaron de ella,
aun es imposible establecer las indicaciones de su uso.
Canalizar
al segundo nivel de atención para la realización de endoscopía a:
- Pacientes con datos de dispepsia no complicada y tratamiento médico, que no presenten mejoría a los 6 meses o que presenten recurrencia de la dispepsia.
- Pacientes con o sin dispepsia y cualquier síntoma de alarma: disfagia, pérdida de peso, anorexia, vomito recurrente ó sangrado digestivo, independientemente de la edad.
- Pacientes con edad > 55 años y presencia de factores de riesgo que presenten dispepsia no complicada de reciente aparición.
- Pacientes con diagnóstico histopatológico de Adenocarcinoma Gástrico que requieran manejo quirúrgico y/o médico y que no puedan ser manejados en segundo nivel, porque no se disponga del recurso humano, material o de medicamentos
Se
deberá de realizar un seguimiento (historia clínica y examen físico completos,
citometría hemática y química sanguínea; los estudios de imagen y endoscopia
solo si clínicamente están justificados) a todos los pacientes cada 4 a 6 meses
los primeros 3 años y posteriormente anual
Se
recomienda un seguimiento de cada 4 a 6 meses los primeros 3 años y
posteriormente anual, deberá de incluir historia clínica y examen físico
completos, citometría hemática y química sanguínea
La
realización de estudios de imagen y endoscopia se deberá de realizar en caso de
sospecha de recurrencia.


















No hay comentarios.:
Publicar un comentario