APNEA OBSTRUCTIVA DEL SUEÑO
La
Organización Mundial de la Salud, a través de la Alianza contra las
Enfermedades Respiratorias (GARD), reconoce que el sindrome de apnea
obstructiva del sueño (SAOS) es una de las enfermedades respiratorias crónicas
más comunes en los adultos, afectando a alrededor de cien millones de personas
en el mundo.
Si bien
el SAOS está fuertemente asociado a la obesidad, es un factor de riesgo
independiente para presentar: accidentes vehiculares, hipertensión arterial
sistémica, eventos cardiovasculares, alteraciones metabólicas, problemas
cognoscitivos, deterioro de la calidad de vida y muerte prematura.
Los
pacientes con SAOS tienen, en promedio, 7 veces más riesgo de accidentes
vehiculares y su tratamiento por medio de presión positiva en la vía aérea
(continuous positive airway pressure-CPAP-) los reduce.
El
síndrome de apnea obstructiva del sueño (SAOS) se caracteriza por episodios
repetidos de oclusión completa (apnea) o parcial (hipopnea) de la vía aérea
superior durante el dormir. Comúnmente se acompañan de una reducción en la
saturación de oxígeno o un breve alertamiento (arousals)
electroencefalográfico.
Los
episodios de obstrucción de la vía aérea superior inducen síntomas diurnos,
como la somnolencia excesiva diurna y deterioro cognitivo aunado con
alteraciones respiratorias, cardíacas, metabólicas e inflamatorias.
Nombres alternativos: apnea
del sueño, síndrome de apnea del sueño, apnea obstructiva, apnea del sueño
mixta, trastorno respiratorio del dormir, síndrome de hipopnea del sueño,
obstrucción respiratoria de la vía aérea superior.
EI SAOS no debe ser confundido con el síndrome de Pickwick debido a que se trata de un padecimiento diferente, el término correcto es síndrome de hipoventilación obesidad, en el cual un grupo de pacientes muestra apneas del sueño.
La edad
incrementa la prevalencia de SAOS. La prevalencia es de 2 a 3 veces mayor en
los adultos mayores, en comparación con los adultos jóvenes. Es mas frecuente
en los hombres, pero con la llegada de la menopausia la prevalencia entre
hombres y mujeres es similar.
Los
pacientes con alto riesgo que deben ser evaluados para síntomas de SAOS son:
- Obesos (IMC 230 kg/m²),
- Con insuficiencia cardíaca, fibrilación auricular, cardiopatía isquémica, hipertensión arterial sistémica refractaria, arritmias cardiacas nocturnas
- Diabetes mellitus tipo 2
- Antecedente de eventos vasculares cerebrales o ataque isquémico transitorio
- Hipertensión pulmonar
- Choferes o conductores de vehículos
- En la evaluación preoperatoria para cirugía bariátrica
Las
mujeres con obesidad en edad fértil deberán ser evaluadas por la presencia de
síntomas de SAOS, ya que se incrementa al doble el riesgo de preeclampsia y
diabetes gestacional.
El
diagnóstico de SAOS se basa en los síntomas y hallazgos clínicos obtenidos en
una historia clínica completa. Ningún parámetro clínico, en conjunto o aislado,
tiene la suficiente exactitud para diagnosticar SAOS.
Los síntomas más frecuentes en SAOS que se deben interrogar en un paciente con alta sospecha son:
- Somnolencia excesiva diurna
- Sueño no reparador
- Cefalea matutina
- Disminución de la memoria de trabajo y de la concentración
- Disminución de libido.
- Irritabilidad, depresión
- Fatiga crónica
- Ronquido habitual
- Apneas presenciadas
- Diaforesis nocturna, insomnio
- Sintomas de reflujo gastroesofágico
El
ronquido habitual es el síntoma más común y que posee la mayor sensibilidad, ya
que se encuentra presente hasta en 95% de los pacientes con AOS. Sin embargo, tiene
un bajo valor predictivo positivo por la alta prevalencia del ronquido en la
población general. La presencia de ronquido como único síntoma no es suficiente
para llevar a cabo un estudio de sueño para diagnóstico de SAOS.
La
presencia de apneas durante el sueño es el síntoma con la mayor especificidad,
la cual aumenta a mayor número de apneas y tiempo de duración.
Es
necesaria una evaluación clínica exhaustiva, ya que nos permite clasificar a
los pacientes en probabilidad preprueba baja, mediana o alta, ayudándonos a
seleccionar el método terapéutico adecuado.
El uso
de la escala simplificada Sleep Apnea Clinical Score (cuello ajustado) mejora
el rendimiento clínico (1-15% la sensibilidad y especificidad) en pacientes con
sospecha de SAOS y permite agruparlos en alta (>48 cm), intermedia (43 a 48
cm) y baja probabilidad (<43 cm).
Medir la circunferencia del cuello en centímetros (cm), si tiene hipertensión arterial (actual o antecedente) sumar 4 cm, si tiene ronquido habitual sumar 3 cm y si le han observado apneas, ahogos o falta de aire cuando duerme agregar 3 cm (Escala 3 del Anexo 5.3).
La
medición de la somnolencia puede ser realizada mediante métodos objetivos y
subjetivos. La somnolencia diurna excesiva es útil para no discriminar a las
personas con SAOS de otras poblaciones, ya que entre 30% a 50% de la población
general reporta algún grado de somnolencia. La gravedad de la somnolencia
excesiva diurna (SED) se correlaciona débilmente con SAOS.
Utilizar
la escala de Somnolencia de Epworth es práctico, considerar una puntuación 210
como sugestiva y 212 como anormal. Esta escala tiene limitaciones y no
discrimina apropiadamente de fatiga y síntomas de depresión.
La
polisomnografía estándar (PSG) se considera el modelo de referencia para el
diagnóstico de SAOS, se realiza durante el horario habitual de sueño del
paciente en un laboratorio del sueño con la asistencia de personal
especializado.
También
es necesaria para el ajuste de la terapia con presión positiva (CPAP).
Los
estudios de PSG durante el día pueden realizarse en trabajadores de turno
nocturno o en otras personas que por lo general están despiertas en la noche y
duermen durante el día. El protocolo y la duración del estudio son los mismos
que los establecidos en el protocolo de noche.
Es
recomendable el registro de dióxido de carbono exhalado en los pacientes con
SAOS, sobre todo si se trata de pacientes con obesidad mórbida (IMC ≥40).
Los
pacientes deben abstenerse de ingerir cafeína en la tarde y noche del día en
que la PSG se ha programado. El alcohol es una cuestión más compleja, debido a
que por la ausencia de alcohol en la noche de PSG podría dar un resultado falso
negativo, si el paciente habitualmente consume alcohol por la noche. Sin
embargo, por cuestiones de seguridad de los pacientes (beber y luego manejar
para llegar al laboratorio, o bien permitirles que beban en el laboratorio y
tener un paciente intoxicado en el laboratorio) no es conveniente, por lo que
tomando estas consideraciones se recomienda que los pacientes eviten el alcohol
el día de la PSG. Los pacientes deben continuar con sus medicamentos habituales
en la noche de PSG, incluyendo pastillas para dormir. Los medicamentos deben
ser anotados por el técnico de manera que los resultados puedan ser
interpretados de manera óptima. Esto es especialmente importante si una
benzodiazepina es uno de los medicamentos, ya que las benzodiazepinas pueden
exacerbar el SAOS.
El
diagnóstico de SAOS se estable cuando el índice de apnea hipopnea (IAH) es 215,
aun en individuos asintomáticos, o cuando el IAH es 25 en combinación con
síntomas propios de la enfermedad y no explicados por otra causa.
La
gravedad del SAOS se define como leve con IAH 25 y <15, moderado con IAH
entre 15 y <30, y grave para IAH >30 por hora de sueño.
En
adultos mayores (265 años) se recomienda que el IAH para diagnosticar SAOS
independientemente de los síntomas. La información disponible muestra sea 210,
que las características clínicas, fisiopatología, diagnóstico y tratamiento es
el mismo que en los adultos jóvenes.
La
literatura disponible demuestra, en general, que un monitor portátil (MP),
también conocido como estudio simplificado, puede ser tan exacto como la PSG
para el diagnóstico de SAOS, pero en poblaciones con alta probabilidad
preprueba de SAOS moderado a grave y que no tengan comorbilidades, como
antecedente de enfermedad vascular cerebral, insuficiencia cardíaca,
enfermedades neuromusculares y EPOC, como mínimo deberá contar con registro de
flujo respiratorio, esfuerzo respiratorio y pulso-oximetria.
En
virtud la gran cantidad y diversidad en las señales de registro de los MP
disponibles comercialmente, se recomienda verificar su calidad en términos de
validación clínica y respaldo tecnológico local.
La
colocación de los sensores deberá ser llevada a cabo por un técnico
especializado.
El
registro de las señales deberá ser revisado y calificado manualmente por un
médico especialista con experiencia en trastornos respiratorios del dormir y el
criterio de calificación deberá ser consistente con los estándares de la AAMD.
El
termino Índice de Eventos Respiratorios (IER), en el caso de un monitor
portátil, se refiere al número de apneas + el número de hipopneas entre el
tiempo total del registro en lugar del tiempo total de sueño, como en el IAH
para el caso una PSG. Como resultado los MP pueden subestimar la gravedad de
los eventos, en comparación con PSG.
Las
unidades médicas que sólo dispongan de MP para diagnóstico del SAOS deberán
trabajar en coordinación con una unidad de referencia en la que se disponga de
PSG.
La
gravedad del SAOS está fuertemente relacionada con la probabilidad de presentar
hipertensión arterial sistémica. La mitad de los pacientes con hipertensión
arterial y 80% de los hipertensos arteriales refractarios a tratamiento médico
lo presentan.
Los
pacientes con hipertensión pulmonar con ronquido habitual deberán ser evaluados
para descartar apnea del sueño debido a que, si la presentan, tiene mayor
riesgo de mortalidad que quienes no la tienen.
Los
individuos que serán operados de cualquier cirugía electiva (sedación o
anestesia general) que presenten factores de riesgo para SAOS deberán ser
estudiados previamente debido a que tendrán mayores probabilidades de
complicaciones perioperatorias (hipoxemia posoperatoria, intubación difícil,
obstrucción respiratoria, delirium, edema pulmonar y falla respiratoria).
En
ausencia de tratamiento, los pacientes con SAOS no tendrán resolución
espontánea de la enfermedad, en estudios observacionales y retrospectivos sólo
se ha observado el empeoramiento del padecimiento, aun con la reducción de
peso.
Las
mujeres con obesidad previa al embarazo tendrán mayores probabilidades para el
desarrollo de SAOS durante la gestación. El riesgo de preeclampsia y diabetes
gestacional será mayor. El uso de CPAP puede reducir el riesgo de
complicaciones.
Los
pacientes con diabetes mellitus tipo II que tienen SAOS grave tienen mayor
impacto metabólico, la cronicidad ha mostrado mayores dificultades en el
control glucémico. El diagnóstico y tratamiento con CPAP podría mejorar el
control metabólico.
Estudiar
y tratar a los pacientes con SAOS disminuye los costos directos e indirectos
donde se ha comprobado que los ingresos hospitalarios por cualquier causa se
incrementan ostensiblemente, el ausentismo laboral es mayor, el gasto en el
tratamiento de las complicaciones, accidentes y sus secuelas y lo concerniente
a muerte prematura es significativamente mayor, en comparación con el grupo sin
SAOS.
Hasta
el momento actual no hay medicamento o sustancia específico (local o sistémico)
que sea capaz de controlar el SAOS.
En el
caso del hipotiroidismo, el tratamiento hormonal de restitución disminuye el
IAH; sin embargo, el impacto en el SAOS es impredecible, por lo que
recomendamos hacerles un estudio de control.
La
pérdida de peso tiene un efecto positivo en algunos pacientes con SAOS leve a
moderado, sobre todo si el IMC llega <25 kg/m². a Desafortunadamente, la
duración del efecto es limitada; sin embargo, debe ser na estrategia obligada
en todos los casos.
Asimismo,
se debe recomendar el abandono del tabaquismo, consumo de bebidas alcohólicas y
sedantes, con lo que mejorará la calidad del dormir y disminuirá el ronquido.
Consultar
la NOM-008-SSA3-2010, Para el tratamiento integral del sobrepeso y obesidad.
La
terapia posicional (evitar la posición supina al dormir) con cualquier técnica
tiene efectos positivos en casos excepcionales; el cumplimiento del tratamiento
ha sido pobre. No se recomienda como único tratamiento.
El tratamiento con oxígeno suplementario no es una forma de tratamiento eficaz y tiene efectos secundarios, como la prolongación de las apneas durante el dormir y la hipercapnia. Se reserva su uso para cuando el SAOS es parte del síndrome de hipoventilación obesidad y otras condiciones cardiopulmonares que lo indiquen.
En
todos los casos, se debe recomendar como tratamiento adyuvante los cambios en
el estilo de vida que permitan mejorar la calidad del dormir y disminuyan los
eventos respiratorios, como el ejercicio aeróbico, dieta hipocalórica e higiene
para dormir.
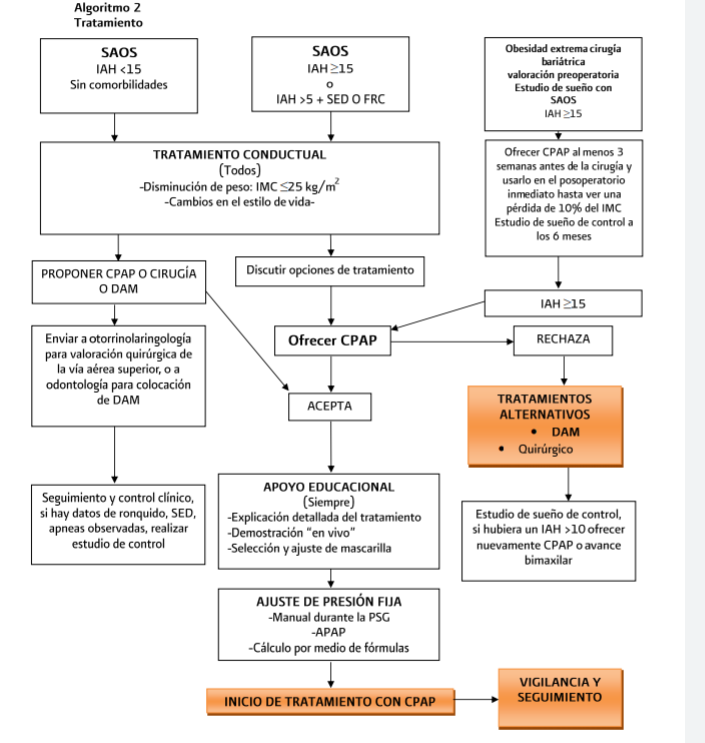
El tratamiento con CPAP nasal durante el sueño está indicado como un estándar en:
- Todos los pacientes con SAOS grave (IAH 230) con o sin SED
- Pacientes con SAOS de leve a moderado (IAH 25) que presentan SED, factores de riesgo cardiovascular
El
tratamiento con CPAP ha demostrado mejorar la calidad de vida y del dormir,
disminuir el estado inflamatorio y el riesgo cardiovascular, disminuir la SED
y, por ende, los accidentes, ya que mejora la capacidad de atención. En la
mayoría de los pacientes mejora la presión arterial sistémica y la presión de
la arteria pulmonar. Asimismo, disminuye la frecuencia de hospitalizaciones por
cualquier causa, como los eventos cardiovasculares fatales y, por lo tanto, la
muerte prematura.
El CPAP
crea una férula neumática en la vía aérea superior que es efectiva para
eliminar el IAH y normaliza la oxigenación sanguínea.
La
terapia con CPAP es segura, los efectos colaterales y eventos adversos son
mínimos y reversibles.
La
única contraindicación absoluta es la fístula de líquido cefalorraquídeo.
La
presión inicial recomendada para una titulación manual es de 4 cm H₂O.
La
presión debe incrementarse en intervalos de por lo menos 5 minutos, de 1 cm H₂O
por ocasión hasta encontrar la presión terapéutica.
La
presión de CPAP máxima recomendada en adultos es de 20 cm H2O.
Una
titulación es óptima si disminuye el IAH a menos de cinco eventos por hora, por
lo menos 15 minutos, que incluya la posición en supino y MOR.
Una
titulación es buena si reduce el IAH a 10 o menos eventos por hora, o en 50% si
el basal es de menos de 15 eventos por hora en supino y en MOR.
Una
titulación es adecuada si no se reduce el IAP a <10 eventos por hora, pero
reduce 75% del IAH basal (especialmente en casos de SAOS grave), o en los casos
de una titulación óptima o buena con la excepción de que no se cumplió la
titulación en MOR y supino.
Una
titulación inaceptable es la que no cumple los criterios anteriores.
Los
pacientes con insuficiencia cardíaca congestiva, enfermedad pulmonar
significativa, pacientes que pueden tener alteraciones del intercambio gaseoso
por una causa diferente a SAOS (como en pacientes con síndrome de
hipoventilación obesidad), pacientes sin ronquido o pacientes con apnea central
no son candidatos para el uso de APAP.
Si la
presión fija de CPAP será obtenida mediante un equipo APAP, se recomienda un
esquema de al menos tres noches para la prescripción. El IAH residual no debe
ser mayor de 10 e idealmente no mayor a 5, las fugas por la mascarilla no
exceder de 0.41/s.
No se
recomienda el uso sistemático de humidificadores, este sistema podría mejorar
el cumplimiento al tratamiento con CPAP en casos en que los pacientes tengan
queja de sequedad de la vía aérea superior.
El uso
de modificación de la curva de presión, por medio de un sistema de liberación
de presión, puede mejorar la comodidad del paciente.
La
mascarilla debe ser acomodada y ajustada ante cualquier fuga no intencional. El
paciente debe saber que la fuga intencional es solamente en el puerto de
exhalación de la mascarilla y que éste tiene el objetivo de eliminar el CO₂
para evitar su reinhalación. Los sitios de fugas no intencionales son a través
de la boca, cuando se usa una mascarilla nasal y entre la cara y la mascarilla.
La
literatura sustenta el tratamiento con CPAP nasal. Sin embargo, algunos
pacientes podrían requerir el ajuste de un BIPAP, como en los casos donde se
requiere una presión alta (CPAP >14 cm de H₂O) y el paciente experimenta
dificultad para la exhalación contra una presión fija.
Los
pacientes con presiones de CPAP >14 cm de H₂O, que toleran la presión y
tienen buen cumplimiento, no deben ser estimulados para el cambio de tecnologia
a BIPAP.
La
presión mínima recomendada de IPAP y EPAP es de 8 y 4 cm H₂O, respectivamente.
La
presión máxima de IPAP recomendada es de 30 cm H₂O.
La
presión diferencial o soporte IPAP-EPAP mínima recomendada es de 4 cm H₂O y la
máxima de 10 cm H₂O.
El tratamiento
quirúrgico incluye una variedad de procedimientos reconstructivos de la vía
aérea superior, únicos o por etapas.
En
todos los pacientes que serán sometidos a tratamiento quirúrgico para el SAOS
son obligatorios el estudio de sueño (PSG o simplificado), previo al
procedimiento, y una evaluación preoperatoria médica (riesgo quirúrgico y
anestésico) y psicológica, con el fin de minimizar los riesgos ante la
intervención quirúrgica.
Los
pacientes deben ser informados sobre las expectativas de éxito, las
complicaciones perioperatorias y la disponibilidad de otras formas de
tratamiento, como el CPAP y los dispositivos de avance mandibular (DAM).
EI SAOS
es una enfermedad compleja, sistémica y que en algunas ocasiones la causa
predominante es la faringe, lo que se conoce como obstrucción fija, para
diferenciarla del paciente con predominio del colapso faríngeo por obesidad y
otros factores de colapso. La mayoría de los pacientes muestra ambos
componentes.
La
recomendación de un tratamiento quirúrgico debe identificar con precisión el
efecto predominante de una obstrucción fija para tener mayores probabilidades
de éxito.
El
tratamiento quirúrgico está indicado en SAOS leve a moderado, en quienes es
clara la obstrucción (hipertrofia amigdalina, velofaringe redundante y
tumores).
El
tratamiento quirúrgico es una segunda línea de tratamiento en pacientes que han
tenido bajo cumplimiento al tratamiento con CPAP y en quienes no tuvieron un
buen resultado con un DAM.
Los
pacientes que tienen una obstrucción fija en la faringe que impide el uso
apropiado del CPAP podrían tener un mejor cumplimiento con un procedimiento
quirúrgico.
El
resultado esperado con el tratamiento quirúrgico es la resolución de los signos
y síntomas, la normalización de la calidad de sueño, del IAH y de los niveles
de oxigenación sanguínea. Por lo tanto, es obligatorio el estudio de sueño
posoperatorio.
Si el
IAH preoperatorio es 215, es recomendable el uso preoperatorio de CPAP, con el
propósito de disminuir el edema de la VAS, mejorar la presión arterial, la
oxemia y la actividad simpática, con lo que disminuirán las probabilidades de
complicaciones con la intubación y curso de la anestesia.
Cirugía de nariz
Septumplastia
y remodelación de cornetes inferiores. Como único procedimiento no se espera la
resolución de la enfermedad.
Uvulopalatofaringoplastia
Es probablemente la cirugía que más se ha realizado como tratamiento en SAOS; sin embargo, la evidencia de éxito como único tratamiento ha sido limitada.
No se recomienda como único tratamiento en pacientes con SAOS moderado a grave.
Se
desaconseja el uso de uvulopalatoplastia con láser, ya que ha mostrado ser
ineficaz.
Los predictores clínicos uvulopalatofaringoplastia son:
1.
Hipertrofia amigdalina grado III y IV 2. Distancia MP-H (mentón hioides) <20
mm
documentada por cefalometría.
3. Sin obesidad
4. Amigdalectomía
La
remoción de las amígdalas como único tratamiento puede acompañarse de buenos
resultados cuando se trata de pacientes hipertrofia grado III y IV. No se
recomienda la reducción del tejido con radiofrecuencia.
Cirugía multinivel o en fases de tratamiento
No
existe información confiable para recomendar su uso, la información existente
se limitada al reporte de series de casos.
La
eficiencia del protocolo de fases quirúrgicas de Fujita no está probada y sus
resultados son impredecibles. Recomendamos la valoración exhaustiva y mesurada
considerando los beneficios contra los riesgos con este abordaje.
La
tecnología para realizar el procedimiento quirúrgico no es determinante en el
resultado, la radiofrecuencia, láser, y otras tecnologías no deben ser
esgrimidas como la fortaleza del resultado quirúrgico.
Implantes de plástico para el paladar
Su
efectividad no está evaluada apropiadamente. Podría ser de utilidad en algunos
casos de SAOS leve o en casos donde el DAM haya sido abandonado.
Avance bimaxilar
Se
puede realizar en los pacientes con SAOS grave que rehúsan a seguir utilizando
el CPAP. Los mejores resultados se han observado en la población joven, sin
obesidad y sin comorbilidades. Es necesaria la intervención de un grupo
multidisciplinario y experiencia quirúrgica para disminuir los riesgos
inherentes al procedimiento.
Traqueostomía
Fue el primer procedimiento utilizado para tratar el SAOS; sin embargo, con el advenimiento del CPAP ha quedado prácticamente en desuso. A menos de que exista una emergencia, no se recomienda su uso hasta no agotar todas las otras opciones.
Si el
especialista y el paciente han considerado realizar la traqueostomía como
tratamiento, se debe tener especial cuidado en contar con las cánulas
apropiadas para pacientes con obesidad.
Las
complicaciones en las cirugías para SAOS son relativamente frecuentes
(obstrucción respiratoria, sangrado e insuficiencia velofaríngea), por lo que
se debe tener especial cuidado en la vigilancia estrecha del posoperatorio.
Colocar
un CPAP y mantener la posición en semifowler en el posoperatorio inmediato es
una medida de seguridad para evitar la obstrucción respiratoria. Vigilar
también el control del dolor y la oxigenación.
La
cirugía bariátrica es un tratamiento adyuvante para SAOS, cuando los pacientes
tienen un IMC 240 kg/m² o un IMC 235, el régimen dietético ha fracasado y
existen comorbilidades relevantes.
Desde
el punto de vista de la reducción en el IAH, la cirugía bariátrica cura el SAOS
en alrededor de 40% de los casos.
El uso
de CPAP posoperatorio en los pacientes operados de cirugía bariátrica no está
contraindicado у si se recomienda utilizarlo para disminuir las posibles
complicaciones y obstrucción respiratoria.
Los DAM
reducen el ronquido y las apneas obstructivas mediante la ampliación del
espacio respiratorio en la base de la lengua y la tensión de los músculos
faríngeos.
Están
recomendados en pacientes con SAOS leve a moderado y en aquéllos con bajo
cumplimiento al CPAP que tengan un IAH <30
Los
predictores clínicos de buen cumplimiento al tratamiento (77% a 1 año, 6.8
horas por noche) con DAM son los jóvenes, con estado dental adecuado y sin
obesidad.
La
evaluación y colocación debe ser realizada por especialistas para el control y
manejo de los efectos secundarios (dolor en la articulación temporomandibular,
dental, salivación excesiva y cambios oclusales), los cuales son temporales.
La
obstrucción nasal crónica puede influir negativamente en el cumplimiento y
beneficio al tratamiento con DAM. En estos casos se recomienda la referencia al
otorrinolaringólogo para su valoración.
Mantener
un seguimiento estructurado favorece el apego al tratamiento, y ayuda al
clínico a identificar cuándo hay mal control de la enfermedad.
Las
consultas de seguimiento se recomiendan al 1er mes de tratamiento, cada 3 meses
durante el primer año, cada 6 meses en el segundo año y desde entonces
anualmente.
Aspectos
que deben ser considerados en el seguimiento de los pacientes con SAOS.
La evaluación
de la somnolencia excesiva diurna, con instrumentos subjetivos como la escala
de somnolencia diurna de Epworth.
- La calidad de vida
- Satisfacción del paciente y del compañero de cama
- Cumplimiento (apego) a la terapia indicada
- Práctica de medidas de higiene del sueño
- Pérdida de peso en pacientes con sobrepeso y obesidad
- Eviitar factores que empeoran la enfermedad, como los hipnóticos, sedantes y alcohol
En
cualquier tratamiento para SAOS, que no sea con un CPAP, el estudio de control
para el seguimiento deberá realizarse con un monitor portátil.
En el
seguimiento de los pacientes que usan CPAP es práctico considerar aquellos con
buen y mal cumplimiento.
Buen
cumplimiento: 24 horas por noche al menos 5 días a la semana.
Mal
cumplimiento: <4 horas por noche y <5 días a la semana.
Como
ocurre con los tratamientos médicos en enfermedades crónicas, el cumplimiento
puede ir disminuyendo.
El hecho de usar una máquina para dormir no reduce
el cumplimiento, si se le compara con pastillas u otras formas de tratamiento. El personal de salud que atienda a los pacientes debe esforzarse por conseguir que el enfermo use todos los días, durante toda la noche, el CPAP.
Cada
vez hay más información que indica el beneficio y reducción de los riesgos a la
salud cuando se usa durante toda la noche.
Los
pacientes deben recibir educación acerca del funcionamiento, cuidado y
mantenimiento de su equipo, los beneficios del tratamiento con presión positiva
y potenciales problemas con su equipo.
El
apego al tratamiento con presión positiva debe ser vigilado, idealmente, en
forma objetiva por medio de los sistemas para medir el uso del dispositivo
(cronómetros o tarjetas de datos).
Cuando
no se ha alcanzado un uso adecuado de la terapia con presión positiva, la
adición de un sistema de humidificación y un programa educacional puede ayudar
a mejorar el uso de CPAP.
El
seguimiento es especialmente importante durante las primeras semanas de
tratamiento con presión positiva, ya que es la oportunidad de resolver
problemas relacionadas con los dispositivos y lograr patrones de utilización
efectiva.
Después
de que un adecuado tratamiento con CPAP se ha instalado y se ha vigilado en el
corto plazo, se recomienda que personal de salud apropiadamente entrenado
realice el seguimiento en forma anual, revisando los objetivos del seguimiento
en cada visita o para resolver problemas acerca de la mascarilla o la máquina.
Situaciones
por las que se debería hacer un estudio de control.
- Cambios sustanciales del peso corporal (>10%)
- Respuesta clínica insuficiente
- Cuando los síntomas vuelven a presentarse luego de una respuesta inicial satisfactoria
En
pacientes tratados que permanecen con los síntomas controlados y no presentan
cambios sustanciales en el peso, no se indica el seguimiento rutinario con PSG
o una poligrafía cardiorrespiratoria.
Cuando un paciente con SAOS moderado o grave fue tratado por cirugía, y después de un período apropiado de cicatrización, debe recibir evaluación de seguimiento que incluya:
Medición objetiva de la presencia y gravedad del SAOS y saturación de oxígeno, ya sea con PSG o poligrafía cardiorrespiratoria Evaluación clínica de síntomas residuales.
Asimismo, los pacientes deben ser seguidos en el tiempo para detectar la recurrencia de la enfermedad y verificar que los factores de riesgo están controlados.
Pacientes
que hayan recibido tratamiento quirúrgico o DAM, que tengan un IAH >5 con
SED o riesgo cardiovascular deberán seguir tratamiento con CPAP, y los que
tengan un IAH >14, independientemente de la presencia de síntomas.
Lo siguiente es competencia del médico en el primer nivel de atención:
Conocer la frecuencia e importancia de la enfermedad
Conocer los factores de riesgo y manifestaciones clínicas de la enfermedad
Usar
herramientas clínicas que le ayuden a identificar a los pacientes con alto
riesgo de la enfermedad
Con
base en los puntos previos, referir al paciente con alto riesgo de apnea
obstructiva del sueño al servicio de neumología del siguiente nivel de
atención, en el que se disponga de los recursos diagnósticos para la enfermedad
Referir
nuevamente al paciente que, una vez con el diagnóstico y el tratamiento instalados,
presente manifestaciones de la enfermedad
Controlar
y vigilar las comorbilidades crónicas del paciente con apnea obstructiva del
sueño, haciendo énfasis en las cardiovasculares y control de peso
Lo siguiente es competencia en el segundo nivel de atención:
Reconocer a los pacientes que puedan ser diagnosticados mediante un estudio de poligrafía respiratoria, es decir:
O Con alta probabilidad clínica de tener la enfermedad
O Sin comorbilidades cardíacas respiratorias o neurológicas significativas que requieran de una PSG Solicitar estudio de sueño simplificado a pacientes que reúnan las condiciones para ello.
Con
base en el resultado del estudio de sueño y los datos clínicos del paciente, se
identificará a quienes deben recibir tratamiento con un dispositivo de presión
positiva y se les ofrecerá
Identificar
y referir al neumólogo del tercer nivel de atención a los pacientes que por su
complejidad requieran de una PSG
En el
caso de neumólogos en el segundo nivel de atención que no dispongan de la posibilidad
de solicitar un estudio simplificado de sueño y ofrecer tratamiento con presión
positiva, deberán referir al neumólogo en el tercer nivel.



























No hay comentarios.:
Publicar un comentario