Sepsis Nenatal
Las
defunciones en los primeros 28 días de vida se deben a trastornos y
enfermedades asociados a la falta de atención de calidad durante el parto o de
atención por parte de personal calificado, así como de tratamiento
inmediatamente después del parto y en los primeros días de vida. Los partos
prematuros, las complicaciones relacionadas con el parto (incluida la asfixia
perinatal), las infecciones neonatales y los defectos congénitos ocasionan la
mayor parte de las defunciones de los RN Dos factores principales explican este
alarmante patrón: en primer lugar, las principales causas de muerte neonatal
integradas por la prematuridad (35%), las complicaciones relacionadas con el
parto, incluida la asfixia perinatal (24%), infecciones neonatales como la
sepsis y la meningitis (15%), la neumonía (6%) y los defectos congénitos (11%),
que causaron la mayor parte de las defunciones del RN en 2016; en segundo lugar
e igual de importante, es la falta de enfoque global en el desafío para poner
fin a la mortalidad neonatal
Se
carece de una definición por consenso para la sepsis neonatal, sin embargo, en
la mayoría de los textos se simplifica como un síndrome clínico en un nacido de
28 días de vida o menos, que se manifiesta por signos sistémicos de infección
venosa y aislamiento de un patógeno bacteriano del torrente sanguíneo. La
sepsis, es la tercera causa de mortalidad neonatal, solo detrás de la
prematuridad y complicaciones relacionadas con el parto (asfixia al nacer).
Los RN, especialmente los prematuros, son más
susceptibles a las infecciones que los niños en cualquier otro período de edad
La
inmunidad innata se ve afectada por el deterioro de la producción de citocinas,
la disminución de la expresión de las moléculas de adhesión en los neutrófilos
y una respuesta reducida a los factores quimiotácticos. Además, el paso
transplacentario de anticuerpos comienza durante el segundo trimestre y alcanza
su máxima velocidad durante el tercer trimestre, como resultado, la mayoría de
los prematuros tienen respuestas humorales significativamente reducidas.
Aunque
los avances médicos recientes han mejorado la atención neonatal, aún quedan
muchos desafíos en el diagnóstico y manejo de las infecciones neonatales. El
diagnóstico de la sepsis neonatal se complica frecuentemente por la presencia
de condiciones no infecciosas que se asemejan a la sepsis y por la ausencia de
pruebas diagnósticas óptimas, especialmente en los RN prematuros. Además
existen complicaciones por sepsis neonatal, que aumentan la morbimortalidad y
la discapacidad a corto y largo plazo, una de las más importantes que requiere
un apartado por su diagnóstico, manejo y pronóstico, es el choque séptico
neonatal.
El
choque séptico puede definirse como un subconjunto de la sepsis, en el que
existen graves alteraciones circulatorias, celulares y metabólicas asociadas a
un mayor riesgo de mortalidad, caracterizado por variables clínicas,
hemodinámicas y de utilización de oxigeno un estado fisiopatológico
caracterizado por un desequilibrio entre el suministro de oxígeno y la demanda
de oxigeno de los tejidos, lo que conduce a hipoxia tisular
Existe mayor variabilidad en las alteraciones
hemodinámicas en el RN, los factores que contribuyen a esta variabilidad
incluyen la estructura y la función alterada de los cardiomiocitos, la
capacidad limitada para aumentar el volumen sistólico, la contractilidad y la
transición de la circulación fetal a la neonatal.
La
sepsis neonatal, a pesar de las estimaciones de la incidencia de casos a nivel
mundial, el mayor riesgo de complicaciones y la discapacidad a largo plazo
recibe poca inversión para su investigación. Se están realizado esfuerzos para
prevenir la sepsis neonatal y su manejo ambulatorio en pacientes no críticos o
que no pueden ser referidos a centros hospitalarios.
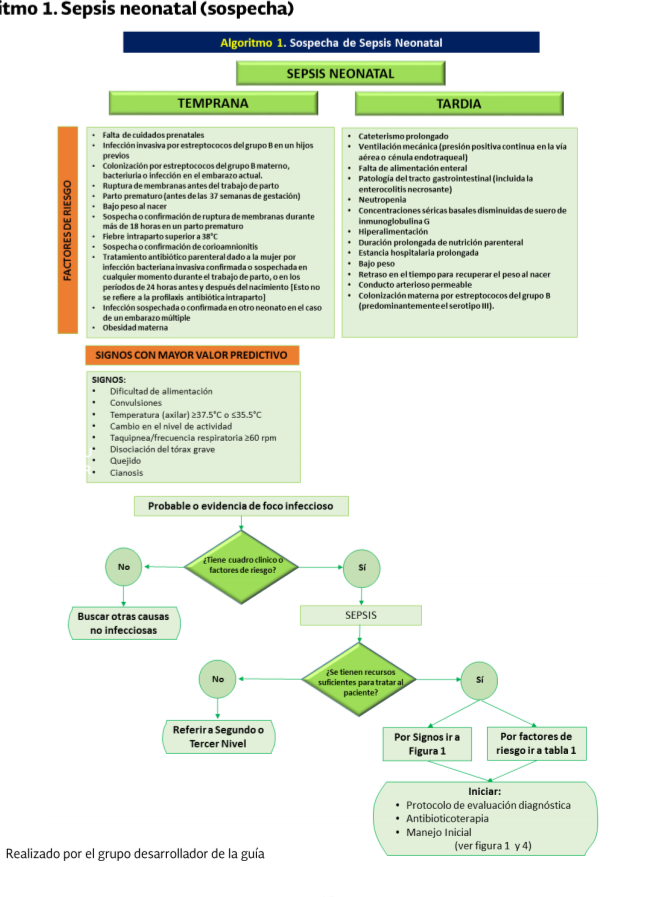
Existen
diversos criterios clínicos para establecer la sospecha sepsis: el grado de
manifestación clínica es muy variable, es dependiente de la virulencia del
patógeno y de los mecanismos de defensa del huésped.
Aplicar
modelos de predicción clínica para iniciar el tratamiento empírico, aumentan la
sensibilidad y especificidad del diagnóstico de sepsis neonatal considerando
los datos más relevantes como:
- Dificultad de alimentación
- Convulsiones
- Temperatura axilar 237.5 Cos 35.5 "C
- Cambio en el nivel de actividad Taquipnea (frecuencia respiratoria 260 rpm)
- Disociación torácica grave
- Quejido
- Cianosis.
Considerar
como indicador de sepsis neonatal, que justifica la toma de hemocultivos e
inicio de antibiótico empírico, a la presencia de tres o más signos clinicos en
un RN con sospecha de infección:
- Convulsiones
- Somnolencia o inconsciencia
- Disminución de la actividad o abombamiento de la fontanela
•
Respiratorio
- Frecuencia respiratoria 260 rpm
- Quejido
- Tiraje torácico grave
- Cianosis central
- Alteración en la perfusión distal (tiempo de llenado capilar >3 segundos
- palidez, aspecto marmóreo, diferencia entre la temperatura central y periférica >2 "C) o pulso rápido y débil
•
Gastrointestinal
- Ictericia
- Dificultad para alimentarse (rechazo alimento)
- Intolerancia alimentaria
- Distensión abdominal
- Emesis
Dermatológico.
- Pústulas
- Eritema periumbilical o purulencia
•
Musculoesquelético:
Edema o eritema que recubre huesos o
articulaciones
•
Sintomas generales:
Tono muscular alterado (flacidez)
Otros:
- Temperatura de 38°C o menor a 36'C
- Acidosis metabólica o déficit de base 210 mmol/l
- Disminución del gasto urinario
Hasta
no contar con estudios en nuestra población, se recomienda no sustituir los
criterios clínicos ya establecidos por algoritmos clínicos electrónicos (ACE)
para determinar el riesgo de sepsis neonatal temprana (SN) y la necesidad del
inicio de antibiótico.
Aunque
pueden ser herramientas útiles, cuentan con limitaciones técnico-tecnológicas,
poca evidencia para sustentarlos y no cuentan con datos de costo efectividad o
con la validación como prueba diagnóstica que justifiquen su uso en nuestro
medio.
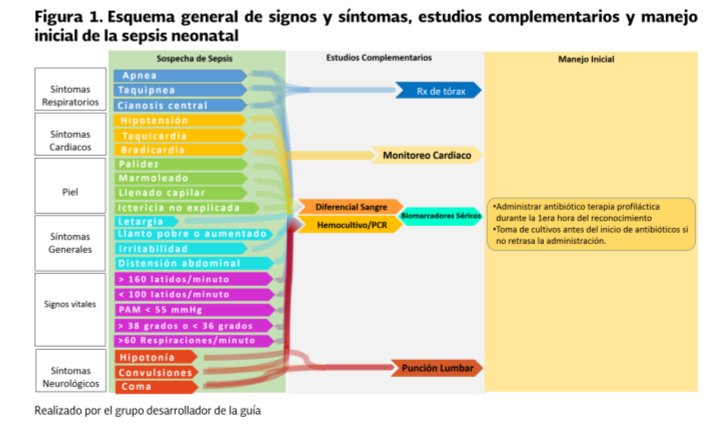
El
hemocultivo es considerado el estándar de oro, Se debe realizar hemocultivo
para determinar el diagnóstico definitivo de sepsis neonatal (Figura 1)
No
sustituir al hemocultivo como prueba diagnóstica por la PCR ya que la evidencia
disponible no permite determinar su precisión diagnóstica.
El conteo leucocitario para determinar el
diagnóstico probable en sepsis temprana y sepsis tardía
Considerar
el conteo celular leucocitario obtenido entre las 6h y 12 h de nacido como más
predictivo de sepsis temprana que el obtenido inmediatamente después del
nacimiento.
No
emplear el conteo leucocitario por si solo, debe sumarse a los datos clínicos y
factores de riesgo para determinar el diagnóstico probable de sepsis neonatal
En caso
de tener disponibles las pruebas de biomarcadores séricos para sepsis ¿Cuál es
la más útil con respecto a sensibilidad y especificidad, comparándola con
proteína C reactiva, procalcitonina e interleucinas?
Determinar
la PCR (en caso de tenerla disponible) para descartar sepsis neonatal, no para
su diagnóstico, previo al inicio de la ministración de los antibióticos y 18 h
a 24 h posterior al inicio de la presentación.
Determinar
la PCT (en caso de tenerla disponible), para descartar sepsis neonatal, no para
diagnóstico, así como, para definir la conducta del uso de antibiótico.
Determinar
las interleucinas (IL) 6 y 8 (en caso de tenerlas disponibles), como apoyo
junto con los datos clínicos para el diagnóstico de sepsis. Existen otras IL
pero la evidencia no permite dar una recomendación En nuestro medio las IL se
utilizan con mayor frecuencia para fines de investigación, por su poca
disponibilidad,
¿Son obligatorios
la punción lumbar, los urocultivos y los aspirados bronquiales para realizar el
diagnóstico y definir el tratamiento en los neonatos con sospecha de sepsis
neonatal?
Realizar punción lumbar (PL) antes de iniciar los antibióticos en pacientes con cuadro clínico sugestivo de meningitis.
Realizar
PL para la toma de muestra de liquido cefalorraquídeo (LCR) en neonatos que no
se realizó PL inicial y que estén recibiendo antibióticos, si presentan:
•
Concentración de proteina C reactiva de 10 mg/ o mayor Uno o varios cultivos
positivos Si no responde satisfactoriamente al tratamiento antibiótico
No
realizar PL en pacientes asintomáticos con sospecha de infección neonatal
temprana (solo dada por factores de riesgo), si el único signo es la dificultad
respiratoria.
No
tomar urocultivo de rutina como parte del estudio del RN con sospecha de sepsis
neonatal temprana
Realizar
radiografías de tórax o aspirados bronquiales, a criterio médico, en aquellos
pacientes que presenten signos o síntomas respiratorios.
¿Tiene
alguna utilidad la proporción del conteo de neutrófilos inmaduros entre los neutrófilos
totales para predecir sepsis neonatal?
La
relación /T > 0.2 puede ser útil para descartar sepsis neonatal temprana,
sin embargo, no sirve para el diagnóstico. Además de la relación /T, deben
considerarse otros parámetros de la biometría hemática.
Considerar los siguientes datos como factores de riesgo:
- Falta de cuidados prenatales
- Infección invasiva por estreptococos del grupo B en un hijo previo Colonización por estreptococos del grupo B materno.
- bacteriuria o infección en el embarazo actual Ruptura de membranas antes del trabajo de parto Parto prematuro (antes de las 37 semanas de gestación)
- Bajo peso
- Sospecha o confirmación de ruptura de membranas por más de 18 horas en un parto prematuro
- Fiebre intraparto superior a 38 C
Sospecha
o confirmación de corioamnionitis Tratamiento antibiótico parenteral ministrado
a la mujer por:
- Infección bacteriana invasiva confirmada
- Sospecha de infección en cualquier momento durante el trabajo de parto
- En los periodos de 24 h antes y después del nacimiento (no se refiere a la profilaxis antibiótica intraparto)
- Sospecha de infección o infección confirmada en otro
- neonato en el caso de embarazo múltiple Obesidad materna (Figura 3)
El
algoritmo de manejo debe realizarse con base en los factores de riesgo
presentes y enfocarse a la observación o inicio del antibiótico profiláctico.
¿Qué
factores de riesgo se deben considerar para definir la antibioticoterapia en
pacientes con sepsis neonatal tardía?
Considerar
como factores de riesgo para sepsis tardía alguno de los siguientes
- Cateterismo prolongado
- Ventilación mecánica (presión positiva continua en la via aérea o tubo endotraqueal)
- Falta de alimentación enteral
- Patologia del tracto gastrointestinal (incluye enterocolitis necrosante)
- Neutropenia
- Bajo peso
- Inmunoglobulina G basal Hiperalimentación baja
- Nutrición parenteral prolongada Estancia hospitalaria prolongada
- Retraso para recuperar el peso al nacer
- Conducto arterioso permeable Colonización materna por estreptococos del grupo B (predominantemente el serotipo II) (Figura 3)
Con
respecto a la antibióticoterapia empírica en sepsis neonatal temprana ¿Qué
régimen debe preferirse con respecto a la mortalidad, comparando ampicilina más
un aminoglucósido gentamicina o amikacina) contra ampicilina con cefalosporinas
de tercera generación (cefotaxima, entre otras)?
Monitorear las tasas de fracaso terapéutico y los perfiles de sensibilidad a los antibióticos de los microorganismos identificados en cada institución, para guiar de forma más precisa la selección de esquemas antibióticos de primera linea (Figura 2 y 4) (Cuadro 3)
Se
recomienda iniciar en el RN pretérmino y a término como esquema antibiótico
inicial (empírico) para infección neonatal temprana: ampicilina más un
aminoglucósido (gentamicina o amikacina).
Usar
las cefalosporinas de tercera generación en monoterapia o combinadas como
antibióticoterapia de segunda línea.
Agregar
en sepsis bacteriana por gram negativos, otro antibiotico activo contra este
tipo de bacterias (cerepima, cefotaxima o carbapenémico, entre otros).
Indicar
dicloxacilina más gentamicina en sospecha de infección por Staphylococcus
sensibles a meticilina (MS) (pústulas cutâneas extendidas, absceso y onfalitis,
agregado a los signos de sepsis), en lugar de penicilina más gentamicina.
Indicar
vancomicina para recién nacidos con infecciones por Staphylococcus aureus
meticilino resistente (MR) como manejo de primera línea
Actualmente
se están estudiando esquemas para la población que no es posible referir a un
centro de salud u hospital, sin embargo, esta particularidad no
forma parte del alcance de esta guía.
En
caso de no contar con gentamicina o cefalosporinas de tercera generación, Cuál
es la mejor estrategia de antibióticoterapia, comparando combinaciones (sin
gentamicina/cefalosporinas) contra el uso de monodrogas?
Considerar
el uso de amikacina o de piperacilina con tazobactam como monoterapia en los
casos de resistencia conocida al tratamiento estándar.
En
pacientes con infección asociada a cuidados de la salud (IACS) ¿Cuál es el régimen
de antibióticos que se debe considerar como tratamiento?
Se
deben considerar a los microorganismos bacterianos como causantes de la IACS,
para lo cual se pueden emplear diferentes combinaciones, que incluyan
cefalosporinas de 3 y 4a generación (cefotaxima y cefepima, respectivamente,
entre otras), carbapenémico (meropenem, imipenem, entre otros) o vancomicina en
caso de ser oxacilino resistente. Se debe considerar la flora nosocomial y la
susceptibilidad reportada al menos en los últimos 5 años.
*Ertapenem
No de forma empírica pues su espectro no cubre Pseudomonas
En caso
de identificarse Candida spp. debe usarse anfotericina B, de preferencia
liposomal o de dispersión coloidal
En
circunstancias especiales (prematuridad, lesión renal, entre otras) ¿Qué
alternativas de regímenes de antibioticoterapia y ajustes de dosis deben
considerarse?
Se deben ajustar los aminoglucósidos de acuerdo con la función renal
La
ceftriaxona está contraindicada en neonatos a término v prematuros con
hiperbilirrubinemia o que reciban calcio.
Debe ajustarse el tratamiento en pacientes con condiciones especiales al nacimiento: Defectos de pared abdominal (gastrosquisis y onfalocele)
No se
recomienda el uso de ceftriaxona en neonatos con hiperbilirrubinemia, porque
desplaza la bilirrubina de los sitios de unión a la albúmina aumentando la
concentración plasmática no conjugada. La administración concomitante de
ceftriaxona y soluciones que contienen calcio está contraindicada
Utilizar
los cuadros existentes de ajuste de dosis de antibióticos para prematuros,
según la edad gestacional y los días de vida extrauterina.
En
circunstancias especiales (prematuridad, lesión renal, entre otras) ¿Qué
alternativas de regímenes de antibioticoterapia y ajustes de dosis deben
considerarse?
Se
deben ajustar los aminoglucósidos de acuerdo con la función renal
La
ceftriaxona está contraindicada en neonatos a término v prematuros con
hiperbilirrubinemia o que reciban calcio.
Debe
ajustarse el tratamiento en pacientes con condiciones especiales al nacimiento:
Defectos de pared abdominal (gastrosquisis y onfalocele)
No se
recomienda el uso de ceftriaxona en neonatos con hiperbilirrubinemia, porque
desplaza la bilirrubina de los sitios de unión a la albúmina aumentando la
concentración plasmática no conjugada. La administración concomitante de
ceftriaxona y soluciones que contienen calcio está contraindicada
Utilizar
los cuadros existentes de ajuste de dosis de antibióticos para prematuros,
según la edad gestacional y los dias de vida extrauterina.
¿Por cuánto tiempo debe continuarse el antibiótico? y ¿En caso de ser el
resultado del cultivo negativo, por cuanto tiempo debe continuarse?
Se
recomienda continuar el tratamiento por 7 a 10 dias, en caso de ser el
resultado de los hemocultivos positivos o en cultivos negativos, pero con
sospecha de sepsis neonatal temprana sin meningitis.
En RN
con sospecha de infección inicial, con bala probabilidad clinica de infección,
laboratorios normales y hemocultivos negativos, se recomienda suspender el
tratamiento antibiótico entre las 36 y 72 h dependiendo de la disponibilidad de
los resultados microbiológicos.
En caso
de considerar el uso de los antibióticos más allá de las 36 h a pesar de los
hemocultivos negativos, se debe revalorar al paciente cada 24 h, para
considerar suspender los antibióticos
Considerar
suspender los antibióticos a las 36 h en neonatos cuyos niveles de la PCR se
estabilicen, presenten cultivos negativos, la sospecha de infección inicial no
tenga sustento y mejoren sus condiciones clínicas.
¿Qué
terapia adyuvante (inmunoglobulinas, pentoxifilina, factores estimuladores de
colonias de granulocitos, entre otros) pueden considerarse para obtener mayor
beneficio del tratamiento antibiótico?
El uso
de probióticos reduce la incidencia de enterocolitis necrosante y la mortalidad
por sepsis, sin embargo, debido a la falta de consenso sobre la posología, tipo
de probiótico y duración del tratamiento en la sepsis neonatal, no se puede
recomendar como una terapia estándar.
En RN prematuros, se recomienda no administrar profilácticamente inmunoglobulina estándar para disminuir la aparición de sepsis o la mortalidad.
La pentoxifilina puede considerarse, en caso de contar con el recurso, como terapia adyuvante en el RN prematuro con sepsis neonatal
El uso
de factores estimulantes de colonias de granulocitos (G FEC) no debe
considerarse como tratamiento de rutina.
Existen RS con MA que relacionan el uso de lactoferrina o leche materna como profilácticos para prevenir la aparición de sepsis tardía: sin embargo esta guía se limita al tratamiento
Los RN
que sufren de sepsis neonatal enfrentan un mayor riesgo de muerte prematura y
alteraciones neurológicas
Existen
complicaciones a corto plazo:
- Choque séptico Meningitis
- Enterocolitis necrosante
- Sindrome de dificultad respiratoria
- Hemorragia intraventricular
- Leucomalacia periventricular
- Disfunción orgánica múltiple .
Asi
como, complicaciones a largo plazo: Alteraciones en el neurodesarrollo
(dificultad en el aprendizaje,parálisis cerebral)
- Sordera o hipoacusia
- Alteraciones en la visión Ceguera
- Displasia broncopulmonar
Debe
darse prioridad al seguimiento del RN con alteración en el neurodesarrollo,
sobre todo en países de bajos ingresos.
CHOQUE
SEPTICO
El tipo de choque que se presenta en la sepsis neonatal es el distributivo.
El
choque séptico se presenta cuando el GC o las resistencias vasculares
sistémicas están alteradas. Se clasifica en cinco tipos:
- Distributivo Cardiogénico
- Hipovolémico
- Obstructivo
- Disociativo
A
diferencia de la población pediátrica o adulta, la hipovolemia no es una
etiología de choque muy común en los primeros días de vida
La
sepsis causa vasodilatación difusa y altera la perfusión: En niños, es más
frecuente el estado no hiperdinamico: es decir, el gasto cardíaco (GC)
disminuido con resistencias vasculares
sistémicas (RVS) aumentadas.
El
choque distributivo, se caracteriza por lesión en el lecho vascular con
hipovolemia relativa, fuga capilar y vasodilatación, con extracción de oxigeno
disminuida lo que conduce a una mayor saturación venosa mixta,
La
sepsis también puede causar disfunción miocárdica (choque cardiogénico), por lo
que se recomienda evaluar la función cardíaca.
La
disfunción miocárdica, la regulación vascular periférica anormal y la
hipovolemia disminuyen el suministro de oxigeno y de nutrimentos a los tejidos.
¿Cuáles
son los criterios diagnósticos clínicos y hemodinámicos del choque séptico
neonatal?
Iniciar
la evaluación con una historia clinica completa, con especial énfasis en los
factores maternos. perinatales v posnatales
El
choque séptico neonatal puede diagnosticarse por signos clinicos, que incluyen:
- Hipotermia o hipertermia
- Alteración en el estado de alerta Vasodilatación periférica (choque caliente)
- vasoconstricción con llenado capilar 22 seg (choque frio) antes de presentar hipotensión
Frecuencia
cardiaca (FC) limite 590 Ipm o 2160 Ipm: se asocia con incremento de la
mortalidad en RN enfermos (no necesariamente sépticos)
En
particular, el miocardio inmaduro tiene un estado contráctil basal más alto y
mayor sensibilidad a los cambios en la poscarga: por lo tanto, es un estado de
resistencia vascular baja, lo cual adquiere particular importancia al remover
la placenta, ya que en la transición de nacimiento pasa a un estado de
resistencia vascular alta, esto se evidencia por el flujo bajo de la vena cava
superior (VCS), observado en una gran mayoria de los RN durante las primeras 6
a 12 h de vida,
El RN
tiene mayor variabilidad en las alteraciones hemodinámicas, los factores que
contribuyen son la estructura y la función alteradas de los cardiomiocitos, la
capacidad limitada para aumentar el volumen sistólico y la contractilidad asi
como la transición de la circulación fetal a la neonatal
Se debe
iniciar prostaglandina E1, en infusión, hasta que se descarte cardiopatia
congenita compleja dependiente de conducto en cualquier RN con choque que presente:
- Hepatomegalia Cianosis
- Soplo cardíaco
- Diferencia en la tensión arterial y en la intensidad de los pulsos entre las extremidades superiores e inferiores (Algoritmo 2)
En el RN, es importante distinguir el choque séptico del cardiogénico, causado por el cierre del ducto arterioso en cardiopatía congénita compleja ductodependiente ante la sospecha para descartarla, se debe realizar el ecocardiograma.
¿Cuál
es el hallazgo de laboratorio más común encontrado en el choque séptico
neonatal?
La
característica de laboratorio más común en el choque neonatal es la acidosis
metabólica, con disminución del bicarbonato sérico o plasmático y aumento del
lactato.
Otros
hallazgos de laboratorio menos comunes incluyen:
- Anemia
- Tiempos de coagulación prolongados
- Alteración en los niveles de glucosa
- Hiperkalemia
- Aumento en los niveles de transaminasas y bilirrubinas
La
acidosis metabólica en el choque séptico neonatal se debe al aumento del
metabolismo anaeróbico (aumento de la producción de lactato) y la disminución
del aclaramiento de lactato
Deben considerarse los siguientes estudios como básicos ante la sospecha de choque séptico:
- Gases sanguineos arteriales (gasometria) Lactato sérico
- Conteo sanguíneo completo con diferencial
- Química sanguinea
- Cultivos sanguineos de liquido cefalorraquideo, orina u otro foco potencial (ocular. pústulas, lesiones de piel,
- articulaciones, traqueal) Grupo sanguíneo y Rh
Pacientes
neonatos con choque séptico ¿Qué solución debe usarse durante la intervención
aguda, comparando soluciones cristaloides isotónicas (solución salina 0.9% o
Ringer lactato) contra soluciones coloides (albumina)
Se recomienda el uso de cristaloides (solución salina al 0.9% entre otros) en bolos de 10 ml/kg, máximo 40 a 60 ml/kg en la primera hora, evaluando la presencia de hepatomegalia o incremento del patrón respiratorio, para la reposición aguda en pacientes con choque séptico.
El
cristaloide es generalmente preferido sobre la albúmina ya que se asocia con
menor riesgo de retención de líquidos.
El
cristaloide es preferido sobre las gelatinas para la restitución en pacientes
con sepsis o choque séptico.
¿Cuál
es el beneficio clínico de usar corticosteroides contra no usarlos durante el
manejo de choque séptico neonatal?
No
deben de usarse de rutina los corticoesteroides en neonatos que responden a
liquidos, vasopresores o terapia antibiótica.
Se
podria considerar el uso de HC en pacientes refractarios a líquidos y terapia
vasoactiva, sin embargo, esta recomendación está basada en estudios de nivel
bajo, por lo cual, no se considera usarlos rutinariamente.
Los
corticosteroides mejoran la fuga capilar en la sepsis (choque distributivo),
por lo tanto, pueden aumentar el volumen circulante glucocorticoide, es el
esteroide más estudiado, generalmente se ministra de 2 a 4 mg/kg/dia (dosis de
carga de 2 mg/lg. seguido de 2 mg/kg/día, dividido cada 12 0 6 h), sin embargo,
los estudios en neonatos con choque séptico no comentan los casos por separado,
son estudios con pocos pacientes, por lo que no es posible establecer una
recomendación basada en evidencia
La terapia con HC se debe agregar si se demuestra insuficiencia suprarrenal en el RN
¿Cuáles
son los datos clínicos a considerar en un choque séptico refractario a
líquidos?
Durante
la reanimación inicial con líquidos, además de los datos de hipoperfusión, se
deben vigilar los de sobrecarga de volumen (aumento de la taquicardia y del trabajo
respiratorio, presencia de estertores, desaturación y hepatomegalia).
Se debe
continuar con la ministración de líquidos, pero con vigilancia estrecha para
evitar la sobrecarga hídrica, ya que se asocia con mortalidad.
Los
pacientes que al inicio no responden rápidamente a los bolos de líquidos o
aquellos con reserva fisiológica insuficiente, se les debe realizar monitoreo
hemodinámico invasivo (colocar catéter venoso central, linea arterial y catéter
vesical).
En pacientes
que requieren vasopresores y en caso de contar con los recursos ¿Cuál agente en
comparación de dopamina contra otros agentes puede considerarse?
El uso
de vasopresores debe individualizarse en relación con la fisiopatología (deseo
de modular las resistencias vasculares pulmonares o sistémicas), la experiencia
y disponibilidad en el centro.
Cuando
es necesario el uso de fármacos vasopresores, deben iniciarse tan pronto como
sea posible, pero dentro de los 60 minutos posteriores a la reanimación,
utilizando un acceso intraóseo o venoso central,
Los
agentes vasopresores e inotrópicos ayudan a revertir la insuficiencia de
ventrículo derecho a través de la reducción de las presiones de la arteria
pulmonar, frecuentemente es necesario en RN con choque refractario a líquidos e
hipertensión arterial pulmonar persistente del RN (HPPN),
Debido
a que en la sepsis neonatal el tipo de choque presente es el distributivo, la
dopamina y la adrenalina pueden tener mayor ventaja por sus mecanismos de acción.
La adrenalina, es normalmente benéfica para el manejo de choque en infantes,
pero Davis sus propiedades farmacológicas son menos conocidas en la población
neonatal
En
pacientes que requieren vasopresores, ¿Existe beneficio en usar combinaciones
contra usar monodroga?
Los
pacientes con choque séptico grave requieren de soporte cardiovascular durante
la reanimación con líquidos. Aunque la dopamina se puede usar como droga de
primera línea, se debe considerar su efecto sobre la resistencia vascular pulmonar
La
combinación de dopamina en dosis bajas (<8 mg/kg/min) y dobutamina (hasta 10
g/kg/min), se recomienda de manera Inicial
Si el paciente no responde adecuadamente a estas intervenciones la adrenalina puede iniciarse (0.05 a 0.3 w/kg/min), para restablecer presión arterial y la perfusión
Se
recomienda usar dosis bajas de adrenalina como primera opción en RN con choque
hipodinamico frío.
No se
encontraron estudios de inotropicos y vasopresores especificos para dar
respuesta a esta pregunta: Sin embargo, el grupo considera que es importante
entender el sitio de acción y los efectos hemodinámicos para el manejo de RN
gravemente enfermo con inestabilidad hemodinámica. Los Inotropicos y fármacos
vasopresores de uso común, utilizados en el choque neonatal, mencionados en las
guias actuales, se resumen v presentan en el respectivo anexo.
En pacientes con datos de persistencia de hipoperfusión posterior al inicio de aminas (refractario a aminas). ¿Qué parámetros deben evaluarse para predecir la respuesta a fluidos comparando los
parámetros
dinámicos contra los estáticos?
Al
contrario del uso de pruebas dinámicas en pacientes de más de un mes de edad en
los RN el uso de estas pruebas para determinar la respuesta a fluidos en choque
séptico refractario no se han estudiado, por lo que no las recomendamos.
La
exploración fisica puede no ser suficientemente sensible para detectar cambios
en el patrón hemodinámica, por lo tanto, los pacientes con choque séptico
refractario a volumen se deben considerar las siguientes herramientas
adicionales para su monitoreo:
- Presión de perfusión normal (presión arterial media - presión venosa central) • Diferencia de saturación de oxigeno preductal y posductal S5%
- Saturación venosa central de oxigeno (Svco) 270% (excepto en pacientes con cardiopatía congenita con lesiones mixtas)
- Flujo de vena cava superior > 40 ml/kg/min
- Gasto cardiaco > 150 ml/kg/min
La
información obtenida mediante ecocardiografia funcional puede ayudar a la
selección lógica de medicamentos, dependiendo de la fisiología subyacente y el
efecto hemodinámico deseado.
En
pacientes con persistencia de datos de hipoperfusión posterior al uso de aminas
(refractario a aminas), ¿Cuál es la conducta más acertada para incrementar el
gasto cardíaco?
Tanto
la vasopresina como la terlipresina se pueden considerar como terapia de
rescate en pacientes con choque séptico vasodilatador que no responde a dosis
altas de noradrenalina ni a otros simpaticomiméticos
En RN
con mala función del ventriculo izquierdo y presión arterial normal, la adición
de nitrovasodilatadores o de inhibidores de la fosfodiesterasa tipo I
(milrinona o Imrinona) o de adrenalina (0.05 a 0.3 Mg /kg/min), pueden ser
efectivas para su tratamiento
La
noradrenalina puede ser efectiva para manejar la hipotensión refractaria: la
Svco, debe mantenerse 270% Laterapia inotrópica adicional se debe agregar si
está justificada
Se
deben transfundir con concentrado eritrocitario a los neonatos con hemoglobina
s12 g/dl.
En RNa
término con hipertensión arterial pulmonar persistente, el uso de óxido nítrico
inhalado es a menudo efectivo. Su mayor efecto generalmente se observa a 20
ppm.
Se debe
sospechar de choque refractario a catecolaminas en los RN con las siguientes
morbilidades no reconocidas (dar tratamiento especifico)
Enfermedad
cardiaca obstructiva o cianótica (sensible a prostaglandina E1)
Ducto
arterioso permeable con diámetro interno grande Errores innatos del metabolismo
(con respuesta a infusión de glucosa, insulina o eliminadores de amonio)
Derrame
pericárdico (pericardiocentesis)
Neumotórax
(toracentesis)
Pérdida
continua de sangre (tranfusión y hemostasia)
Hipoadrenalismo
(hidrocortisona)
Hipotiroidismo
(triyodotironina)
La
triyodotironina es un inotrópico efectivo en recién nacidos con insuficiencia
tiroidea
Cuando
las causas anteriores se han excluido. la ECMO se convierte en una terapia
importante a considerar en el RN a término y pretérmino tardio.
Los
trabajadores de la salud de primer contacto o de unidades de medicina familiar
con capacitación limitada o con poca experiencia en el manejo del RN deben
conocer los predictores clínicos de las enfermedades graves y sus diagnósticos
especificos, para referir a estos pacientes al segundo o tercer nivel de
atención
Se
recomienda referir a los RN menores de 34 semanas de gestación y de 1500 g de
peso, al tercer nivel de atención en cuanto se tenga la posibilidad de hacerlo,
por la incidencia de complicaciones a corto plaza



























No hay comentarios.:
Publicar un comentario