GLAUCOMA CONGENITO PRIMARIO
La
Organización Mundial de la Salud considera que la ceguera infantil es el
resultado de condiciones que son prevenibles o tratables, debido a esto, hace
énfasis en las estrategias de prevención; y reconoce que existen condiciones
como el glaucoma congénito primario que requieren de mayores avances médicos
para su control óptimo Debido a la baja
incidencia, el diagnóstico puede pasar desapercibido y retrasarse, lo que trae
como consecuencia tratamiento tardío e inadecuado; además de secuelas.
La
trasmisión genética es heredada a través de un patrón autosómico recesivo y
paralelo a lo anterior, existen reportes con prevalencia alta: en países Árabes
1 en 2,500 y en los gitanos de Eslovaquia 1 en 1,250
El
glaucoma en edad infantil es raro, pero puede llevar a la ceguera cuando es
sub-diagnosticado o tratado de forma sub-óptima; puede ser clasificado como
primario o secundario
El tipo
primario, ha sido reportado como el más común en Europa, Australia, Asia y en
población con factores de riesgo.
La
mayoría de los casos se diagnostican alrededor de los 6 meses y se estima que
el 80% en el primer año de edad. Predomina en masculinos (65%) y usualmente es
bilateral (70%). Esta caracterizado por la falta de desarrollo de la malla
trabecular, sin otra alteración ocular
En
México, los reportes coinciden con la literatura internacional aunque con
cifras menores, esto puede representar una baja incidencia de la enfermedad o
bien una baja frecuencia de diagnóstico, por lo que es importante capacitar al
personal de salud para mejorar la oportunidad del diagnóstico y
consecuentemente reducir las secuelas visuales generadas.
El
glaucoma congénito primario, es un desorden en el desarrollo de la malla
trabecular del globo ocular que se asocia a un incremento en la presión
intraocular (PIO), esta elevación de la PIO causa los cambios característicos
que incluyen, crecimiento anormal del ojo o buftalmos (incremento de la
longitud axial), edema y opacidad corneal, estrías de Haab, aumento del
diámetro corneal, aumento en la excavación y atrofia del nervio óptico, en
ausencia de otra condición ocular o sistémica
The
Childhood Glaucoma Research Network, estandarizó la definición de glaucoma
infantil, la cual requiere dos o más de los siguientes criterios.
- Presión intraocular mayor a 21 mmHg
- Agrandamiento de la copa del disco óptico o asimetría mayor a 0.2 entre los dos ojos
- Datos corneales (estrías de Haab, edema corneal, diámetro corneal horizontal ≥ 11 mm en recién nacidos, > de 12 mm en niños < de 1 año, >13 mm en mayores de 1 año), Miopía o crecimiento axial, o un defecto campimétrico sugestivo de glaucoma
También
existen los niños con sospecha de glaucoma cuando existen los siguientes
criterios aislados:
- PIO mayor a 21mmHg en dos ocasiones
- Apariencia sospechosa del nervio óptico
- Campo visual sospechoso de glaucoma
- Agrandamiento de la copa del disco óptico o del diámetro corneal con PIO normal
Clasificación
del Childhood Glaucoma Research Network y la World Glaucoma Association.
1.
Glaucoma infantil primario
Glaucoma congénito primario
Glaucoma juvenil de ángulo abierto
2.
Glaucoma infantil secundario
Glaucoma asociado con anomalías oculares no
adquiridas
Glaucoma asociado con síndromes o enfermedades
sistémicas no adquiridas
Glaucoma asociado a condiciones adquiridas
Glaucoma después de cirugía de catarata
DATOS CLINICOS
Durante
la exploración en consultorio se recomienda realizar búsqueda intencionada de
córnea opaca, asimetría corneal, fotofobia y lagrimeo en todos los pacientes
menores de 48 meses de edad. (ver anexo 5.3.1)
Se
recomienda realizar exploración bajo anestesiageneral en el quirófano.
Es
indispensable la exploración del segmento anterior a todo paciente con sospecha
de glaucoma congénito y se debe utilizar microscopio para establecer :
- Medición del diámetro corneal horizontal con compás quirúrgico
- Realizar búsqueda intencionada de edema corneal y estrías de Haab
- Valoración de fondo de ojo y gonioscopía cuando la transparencia corneal lo permita
Se
recomienda que durante la exploración bajo anestesia se realice la toma de PIO
en los primeros minutos de exposición al medicamento para reducir la
posibilidad de subestimarla (ver anexo 5.3.2)
La toma de PIO deberá ser la primera actividad durante la exploración bajo anestesia, incluso antes de intubar, cuando así sea posible. Esto permitirá obtener cifras más reales para la toma de decisiones respecto a establecer diagnóstico e iniciar tratamiento.
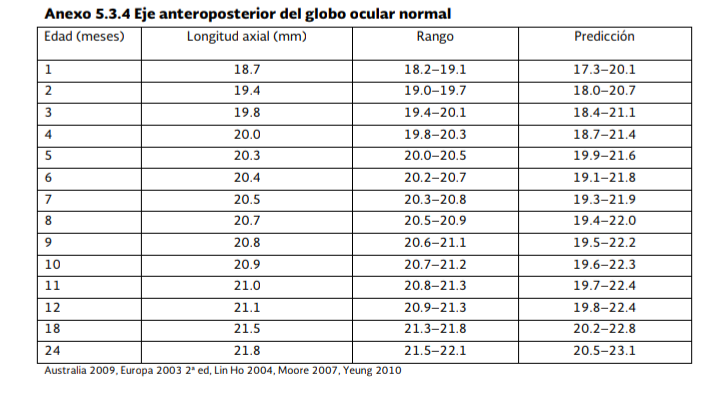
Se
recomienda realizar el análisis de la información obtenida en la exploración
bajo anestesia considerando los anexos 5.3.1 a 5.3.4 que incluyen rangos
normales de diámetro corneal, PIO y eje anteroposterior debido a que las cifras
varían acuerdo a la edad cronológica. Para llegar al diagnóstico definitivo.
Durante
la primera exploración bajo anestesia se debe buscar establecer diagnóstico de
certeza y evaluar la posibilidad de realizar tratamiento quirúrgico en el mismo
evento anestésico, de acuerdo a recursos de la unidad, habilidades y
experiencia del cirujano, buscando obtener reducción de presión intraocular y
posteriormente establecer esquema de seguimiento de acuerdo a resultados.
PRUEBAS DIAGNOSTICAS
El
diagnóstico puede apoyarse en estudios como la ecografía y ecometría; sin
embargo, ninguno de ellos establece el diagnóstico definitivo y tampoco los descarta,
por lo que la clínica sigue siendo el elemento más sólido para el diagnóstico.
Las pruebas deberán realizarse como apoyo para la vigilancia y seguimiento de
los casos .
Los
estudios diagnósticos serán definidos por cada médico tratante, ajustandose a
los recursos de los que se dispone en cada unidad hospitalaria, considerando
que ninguno de ellos establece el diagnóstico definitivo.
Los
pacientes con glaucoma congénito primario que logran control de la PIO tienen
córneas más gruesas que los controles no glaucomatosos. La córnea más gruesa
podría alterar significativamente la medición de la PIO con tonometría de
aplanamiento. La paquimetría debería considerarse como una parte esencial de la
evaluación para el glaucoma congénito primario.
La
paquimetría es un parámetro importante aunque no debe ser utilizado como factor
corrector de la medida de PIO obtenida. Los pacientes con glaucoma congénito
primario o glaucoma juvenil tienden a tener córneas más delgadas, en cambio, en
pacientes con aniridia o afaquia el espesor corneal suele ser mayor que el de
la población normal.
La
evidencia disponible respecto al uso de de la paquimetría es contradictoria por
lo en este momento no debe considerarse para el diagnóstico, hace falta más
investigación al respecto.
TRATAMIENTO
NO FARMACOLOGICO
El
tratamiento médico es destinado a la preparación del paciente previo al
procedimiento quirúrgico y en algunos casos como terapia coadyuvante después de
la cirugía. Las técnicas quirúrgicas usadas dependen del grado y severidad del
glaucoma
1.
Goniotomía: cuando las estructuras del ángulo están visibles
2.
Trabeculotomía: si el ángulo no es visible Si hay falla de estas técnicas es
posible utilizar técnicas similares a los adultos: trabeculectomía o uso de dispositivos
de drenaje. Ciclodestrucción del cuerpo ciliar usando laser.
El
tratamiento del glaucoma congénito primario es de primera intención quirúrgico
y orientado a lograr el control de la presion intraocular; como procedimiento
de primera línea se realiza gonitomía siempre que las estructuras del ángulo
sean visibles; cuando la córnea es opaca y no permite observar las estructuras,
la opción es realizar trabeculotomía simple o combinada.
Los
procedimientos quirúrgicos están orientados a alcanzar niveles de presión
intraocular normales; es importante especificar que los procedimientos deberán
ser decididos por el médico tratante considerando experiencia, habilidades y
recursos materiales disponibles en la unidad hospitalaria; debido a que el
tratamiento de estos pacientes es de por vida, serán necesarios múltiples
procedimientos quirúrgicos donde es primordial conservar la conjuntiva sana,
por lo que se recomienda iniciar con goniotomía o tratamientos en sector nasal.
Procedimientos
de más reciente introducción incluyen: diversas variedades de canaloplastia,
trabectomia, derivación Express y Stent. Estos procedimiento aún no se
consideran de rutina, sus reportes son escasos y de pequeñas poblaciones por lo
que se espera que en un futuro se puedan realizar conclusiones solidas sobre ellos.
La
cirugía ocular bilateral simultanea contínua siendo un punto de controversia y
algunos reportes mencionan ventajas que deben ser consideradas como la
reducción de riesgos por el número de episodios de anestesia general, riesgo de
ambliopía por deprivación y días de hospitalización.
Queda a
consideración del médico tratante la decisión de realizar cirugía bilateral
simultanea de acuerdo a las características sistémicas y oculares individuales
de cada paciente.
TRATAMIENTO
FARMACOLOGICO
El
tratamiento farmacológico está indicado previo al manejo quirúrgico con el
objetivo de disminuir la presión intraocular y evitar el daño secundario. La
cirugía es el tratamiento de elección de estos pacientes. También se indica
como coadyuvante, cuando la reducción de la PIO es insuficiente posterior a la
cirugía.
El
médico podrá indicar cualquiera de los medicamentos que están disponibles para
el control de presión intraocular (excepto brimonidina), tomando en
consideración las características específicas de cada paciente, sus
antecedentes y objetivos a alcanzar.
El uso de brimonidina está contraindicado en
prescolares y niños lactantes con peso menor a 40 libras (aproximadamente) ya
que puede causar bradicardia, hipotermia, hipotonía y cuando se combina con
beta-bloqueadores puede causar apnea de origen central.
La
brimonidina puede ser utilizada en escolares como terapia de segunda y tercera
línea en casos de glaucoma juvenil de ángulo abierto, afaquia y niños mayores
con otro tipo de glaucomas.
El
seguimiento a largo plazo de pacientes con glaucoma congénito primario, ha
revelado un incremento importante en la longitud axial de estos ojos lo que conlleva
un incremento en el riesgo de desarrollo de lesiones degenerativas y predisponientes
en retina, con el consecuente riesgo de desprendimento de retina y mayor
deterioro visual.
La
prevalencia de desprendimiento de retina regmatógeno entre ojos con PCG es
alta. La revisión de retina periférica se debe realizar en los ojos con PCG, especialmente
aquellos que presentan longitud axial de 26 mm o más.
El
procedimiento quirúrgico de elección será decisión del cirujano de acuerdo a
los recursos hospitalarios, experiencia y habilidades del médico tratante.
El
paciente será sometido a cirugía en el tercer nivel de atención, la elección de
la técnica quirúrgica dependerá de la transparencia corneal y de las
alteraciones anatómicas angulares. Se recomienda la siguiente secuencia de
procedimientos:
Goniotomía(s) vs trabeculotomía
Trabeculotomía sola o combinada con
trabeculectomía
Segunda cirugía nueva goniotomía o trabeculotomía combinada con trabeculectomía con o sin anti metabolitos en un sector de ángulo diferente al inicial
Trabeculectomía con o sin anti metabolitos
Implante valvular (es)
Cicloendofotocoagulación
Ciclocrioterapía
Evisceración
Una vez
estabilizada la PIO en el curso del manejo médico-quirúrgico, podrá referirse a
segundo nivel de atención para su vigilancia y tratamiento.
El
paciente contra referido a segundo nivel de atención debe ser valorado a
criterio del médico para realizar tonometría, medición de diámetros corneales,
estado refractivo y evaluación de fondo de ojo en consulta externa o bajo
sedación individualizando a cada paciente.
En caso
de encontrar descontrol de la PIO o evidencia clínica de progresión de la
enfermedad debe ser referido nuevamente a tercer nivel de atención.
La
evalución sistémica y los exámanes de control con pruebas de función hepática
se realizarán previos a evento anestésico y el médico establecera otros
exámenes necesarios para el seguimiento dependiendo del estado general y de las
alteraciones que presente.
Dentro
del seguimiento del paciente pediátrico con glaucoma deberá incluirse rehabilitación
visual, así como la vigilancia del eje antero posterior mediante ultrasonido, y
campos visuales dependiendo de la edad del paciente.
1.-
Envío urgente del primero al segundo nivel de atención en caso de identificar
los siguientes datos en menores de 24 meses:
Lagrimeo
Fotofobia
Blefaroespasmo
2.-
Envío urgente del segundo al tercer nivel después de tener diagnóstico de
certeza corroborado
Aumento del diámetro corneal
Córnea opaca
Evaluación de fondo de ojo
Tonometría
Contra referencia ordinaria del tercero al
segundo nivel de atención de los pacientes operados y estabilizados para
control y seguimiento.























No hay comentarios.:
Publicar un comentario